
(1)三氧化硫(SO3)中,硫元素与氧元素的质量比是_________,硫元素的质量分数是_________.
(2)我市某氯碱工厂排放的尾气里含有毒的氯气(Cl2),为防止其污染空气,工厂用20%的NaOH溶液吸收氯气(反应的化学方程式为Cl2+2NaOH=NaClO+NaCl+H2O).计算:4t溶质质量分数为20%的NaOH溶液,理论上可吸收氯气的质量为多少?
科目:初中化学 来源: 题型:计算题
某化学兴趣小组的同学在实验室配制质量分数为20%的碳酸钠溶液,并完成有关实验。
(1)配制100g质量分数为20%的碳酸钠溶液。
①配制方法A、需要碳酸钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。配制方法B、若用40%的碳酸钠溶液稀释成100克20%碳酸钠溶液,则需取40%的碳酸钠溶液多少亳升?(密度为1.4克/毫升) (填答案)。
②配制溶质质量分数一定的碳酸钠溶液常按以下操作顺序进行。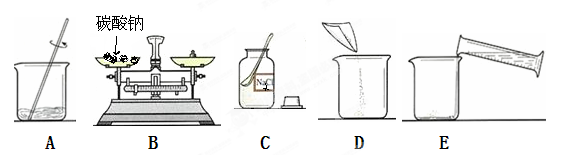
则用上图所示的序号表示正确配制该溶液的操作顺序为 。
③用托盘天平称量所需的碳酸钠时,发现托盘天平的指针偏向左盘,应 。
A.增加适量固体 B.减少适量固体
C.调节游码 D.添加砝码
④分析:以下原因可能导致配到的碳酸钠溶液溶质质量分数小于8%的是( )
A、固体中混有杂质
B、量水时仰视读数
C、配好后装入试剂瓶中时有少量液体洒出
D、量水时俯视读数
(2)取上述配制得到的20%的碳酸钠溶液53克,加入68.4克某浓度的稀盐酸后,恰好完全反应,求反应后所得溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
点燃H2、O2和N2的混合气体20g,充分反应后生成18g水,则剩余的可能是( )
| A.O2和N2的混合气体2g | B.H2和N2的混合气体2g |
| C.H2、O2和N2的混合气体2g | D.2g N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
经过研究发现,对任何气体而言,6.02×1023个分子具有下列定量关系:①其质量在数值上等于该分子的相对分子质量,单位为克;②在压强为1.01×105Pa和0℃时其体积为22.4升。据此可知,32克二氧化硫的分子数为 个,含有的氧原子数为 个,在压强为1.01×105Pa和0℃时其体积为 升。
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
工业上以CaO和HNO3为原料制备Ca(NO3)2?6H2O晶体.为确保制备过程中既不补充水,也无多余的水,所用硝酸的溶质质量分数约为( )
| A.41.2% | B.53.8% | C.58.3% | D.70.0% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
实验室有一瓶浓盐酸,瓶上标签的部分内容如下图所示,请你根据标签上提供的数据解答下列问题: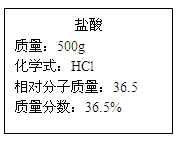
(1)为了证明该瓶盐酸显酸性,你可以采取的做法是 。(简单描述即可)
(2)取出200g该浓盐酸,稀释成18.25%的稀盐酸,需要加入水的质量为 g。
(3)现用刚配好的100g18.25%的盐酸与足量的锌粒完全反应,理论上可以生成氢气的质量是多少?(反应化学方程式:Zn+2HCl= ZnCl2+H2↑)
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素。
(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是 (填序号)。
①KCl; ②NH4HCO3; ③Ca3(PO4)2。
(2)“测土配方”可以实现“缺什么、补什么”,使用该技术的好处是 。
(3)某同学取丰收牌钾肥(如图1)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图2。试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(反应方程式为:K2SO4+BaCl2=BaSO4↓+2KCl,杂质不参加反应。)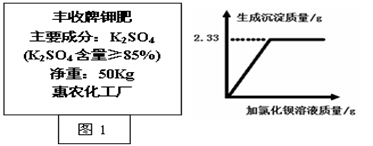
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= .
(2)通过计算,上述过程中同时产生H2的质量为 g.
(3)计算电解后剩余溶液中NaC1的质量分数(写出详细的计算过程,结果精确到0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某长期暴露在空气中的烧碱样品已部分变质,为了测定其纯度,现进行如下实验:取样品18.6g加入到85.8g水中充分搅拌至完全溶解,向所得溶液中逐滴滴加稀盐酸,产生气体的质量与所加稀盐酸质量的关系如图所示。分析题意并回答下列问题: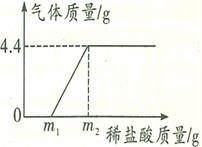
(1)反应过程中生成气体的质量是 。
(2)该烧碱样品中氢氧化钠的质量是多少克(写出规范的解题过程)?
(3)所用稀盐酸的溶质质量分数是 (用ml和m2表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com