小华同学为探究实验室中三种碳酸盐:碳酸氢铵、碱式碳酸铜、碳酸钙的性质,进行了以下实验:
实验1:
小华打开盛放碳酸氢铵固体的试剂瓶,闻到有氨臭气味,用湿润的
红
红
色石蕊试纸检验,试纸变
蓝
蓝
,证明是氨气.
取少量碳酸氢铵固体于试管中,加入少许水振荡.完全溶解后,向溶液中滴入几滴酚酞试液,观察到溶液为无色.将试管放入60℃热水中加热,很快观察到碳酸氢铵溶液中有大量气泡产生,并闻到较浓的氨臭味,同时,溶液由无色逐渐变为红色.
(1)实验证明,碳酸氢铵易分解产生氨气,同时产生另一种气体和水.写出碳酸氢铵分解的化学方程式
NH4HCO3 =NH3↑+CO2↑+H2O
NH4HCO3 =NH3↑+CO2↑+H2O
.
(2)溶液中的酚酞由无色逐渐变为红色的原因是
相同条件下,氨气溶解能力比二氧化碳强,溶液显碱性
相同条件下,氨气溶解能力比二氧化碳强,溶液显碱性
;
(3)小华根据碳式碳酸铜和碳酸钙分解的条件,得出这三种固体的热稳定性由强到弱的顺序是
CaCO3>Cu2(OH)2CO3>NH4HCO3
CaCO3>Cu2(OH)2CO3>NH4HCO3
.
(4)根据实验,小华联想到农村在存放“碳铵”(碳酸氢铵)化肥时应该注意
在阴凉干燥处密封保存
在阴凉干燥处密封保存
.
实验2:
小华各取三种固体试剂少许于试管中,分别加入1mL 1:2的盐酸溶液.观察到三支试管中均有
固体溶解,产生大量气泡
固体溶解,产生大量气泡
的现象,其中,
碳酸氢铵
碳酸氢铵
与盐酸反应的速率最快.
(1)由实验可知,三种碳酸盐均能与稀盐酸反应,写出碱式碳酸铜与盐酸反应的化学方程式
Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑
Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑
.
(2)根据实验现象,你认为实验室
否
否
(能或否)用碳酸钙固体粉末代替石灰石与盐酸反应制取二氧化碳,原因是
碳酸钙粉末与盐酸接触面较大,反应过快,难以收集
碳酸钙粉末与盐酸接触面较大,反应过快,难以收集
.

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案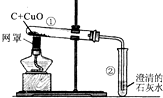 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.