

分析 (1)根据化学反应遵循质量守恒定律可知,在化学反应前后元素的种类和数目及原子的种类和数都不变,则可利用电池中的化学反应借助守恒的方法判断X的化学式.(2)根据金属的性质来分析;
(3)利用化学方程式计算出碳的质量然后在进行二氧化锰质量分数的计算;
(4)根据化合物中元素化合价的计算方法以及方程式的书写方法来分析;
(5)根据改进后的装置特点来分析.
解答 解:(1)由电池工作时反应的化学方程式为:Zn+2MnO2+2NH4Cl═ZnCl2+2NH3↑+X+H2O,可以看出Zn、Cl、H、N四种元素的原子个数在反应前后都相等,而Mn、O两种元素的原子个数反应前后不相等,反应前有2个锰原子,4个氧原子,反应后出现了1个氧原子,所以可以判断则X中应含有2个锰原子和3个氧原子,则X的化学式为Mn2O3.故填:Mn2O3;
(2)锌和汞两种金属的沸点不同,可采用热处理的方法加以分离;故填:沸点;
(3)在加热时,碳生成了二氧化碳,二氧化碳通入石灰水中产生了碳酸钙沉淀.C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+Ca(OH)2=CaCO3↓+H2O,由以上两个化学方程式可知,碳、二氧化碳以及碳酸钙之间的关系为:C~CO2~CaCO3
设碳的质量为x
C~CO2~CaCO3
12 100
x 5g
$\frac{12}{x}=\frac{100}{5g}$
x=0.6g
混合物中二氧化锰的质量分数为:$\frac{2g-0.6g}{2g}×$=70%
答:混合物中二氧化锰的质量分数为70%.
(4)在氯化锰(MnCl2)中,氯元素显-1价,则锰元素显+2价,反应的方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑,故填:+2;4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑;
(5)制成块状固体后,反应物之间的接触面积变小,关闭止水夹时,试管气压增大,将液体压回长颈漏斗,固液分离,反应停止;均能通过控制获取平稳的气流;故填:制成块状固体后,反应物之间的接触面积变小;关闭止水夹时,试管气压增大,将液体压回长颈漏斗,固液分离,反应停止.
点评 本题以信息题的方式考查了物质的分离和提纯,侧重能力的考查.


科目:初中化学 来源: 题型:选择题
 按如图装置进行实验,有关说法及分析不正确的是( )
按如图装置进行实验,有关说法及分析不正确的是( )| A. | 烘干的木炭粉末与CuO粉末须混合均匀 | |
| B. | 网罩的作用是集中火焰,提高温度 | |
| C. | 可观察到澄清石灰水变浑浊 | |
| D. | 结束时先熄灭酒精灯,过一会儿后从液体中取出导管 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
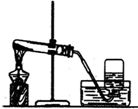 实验室用高锰酸钾制取氧气(如图所示),有以下操作步骤:
实验室用高锰酸钾制取氧气(如图所示),有以下操作步骤:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
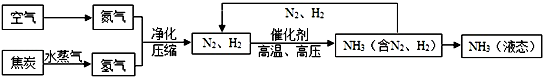
| 物质 | H2 | N2 | O2 | NH3 |
| 沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是用氧化铁炼铁原理的装置图:
如图是用氧化铁炼铁原理的装置图:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
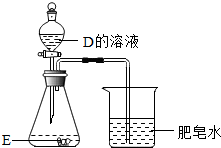 下列字母A~E表示初中化学常见的物质,它们由氢、碳、氧、硫、钠、铁、铜中的1~3种元素组成.
下列字母A~E表示初中化学常见的物质,它们由氢、碳、氧、硫、钠、铁、铜中的1~3种元素组成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com