
【题目】硅是信息技术的关键材料,高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,该反应的化学反应方程式为:2H2 + SiCl4![]() Si + 4X,下列说法正确的是( )
Si + 4X,下列说法正确的是( )
A. X的化学式为HClB. 该反应是复分解反应
C. 四氯化硅是由一个硅原子和四个氯原子构成D. 四氯化硅中硅元素和氯元素的质量比为1:4
 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:
【题目】美国普度大学研发出一种制备氢气的新工艺,流程如图所示。铝镓合金是铝和镓熔合在一起的混合物,具有金属特性。铝镓合金与水的反应中生成物是氧化铝、氢气和镓,相当于镓未参加反应,所以实际上发生的反应是:2Al+3H2O═Al2O3+3H2↑
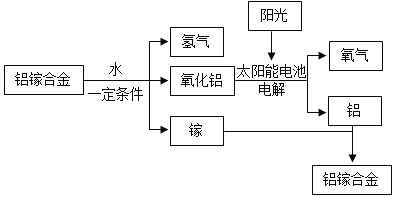
(1)铝镓合金_____导电(填“能”或“不能”)。
(2)铝在常温下能被氧气氧化生成氧化铝,写出该反应的符号表达式_____。
(3)当前工业上常采用电解水制取氢气,反应为2H2O![]() 2H2↑+O2↑,电解水制取氢气需要消耗电能且反应的速度慢,与之相比,由铝镓合金制取氢气的优点是_____。
2H2↑+O2↑,电解水制取氢气需要消耗电能且反应的速度慢,与之相比,由铝镓合金制取氢气的优点是_____。
(4)流程中含有氧元素的物质有_____。
(5)下列说法正确的是_____。
A铝镓合金可以循环利用
B太阳能的利用可以部分解决能源危机问题
C铝镓合金制取氢气的反应属于分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据报道,中国科学技术大学研究人员利用钴及其氧化物成功研制出一种新型催化剂,可将二氧化碳高效“清洁”地转化成液体染料,反应的微观示意图如下。有关该反应的说法正确的是( )
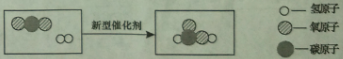
A.反应前后原子总数减少
B.反应物和生成物中共有两种氧化物
C.得到的液体燃料化学式是H2C2O
D.可用于减少温室气体的排放
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E五种物质都是已学化学内容中涉及到的常见物质,其转化关系如下图所示:
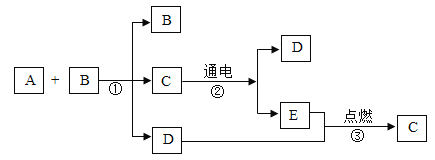
(1)写出下列物质的化学式:
A______________ C _____________ E___________
(2)写出反应①、③的化学方程式,并指出其基本反应类型:
①__________________ ;(_____________)反应 )
③__________________。(______________)反应)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示。
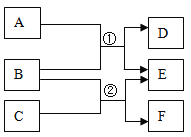
(1)若B是目前世界上年产量最高的金属,D是一种红的单质,F是一种气体,
①写出D物质的一种用途_____
反应①的基本反应类型为_____
②反应②的化学方程式为_____
(2)若A、B、C表示不同类型的化合物,E在常温下是一种无色液体,A中含有两种元素且A能与F发生反应。
①写出一个符合题意的A与F反应的化学方程式____
②A~F六种物质中属于盐的是_____(填字母)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
【猜想】Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气 ,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后 。
【实验】天平称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

⑴ 填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出, 带火星的木条复燃。 |
| 溶液中有气泡放出,
| 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
⑵ 步骤①的目的是 。
步骤⑦的目的是 。
⑶ 过氧化氢能被氧化铜催化分解放出氧气的文字表达式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】欲配制100 g 10%的NaCl溶液,操作如图所示。
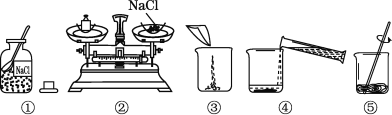
请回答下列问题:
(1)图中操作有错误的是________(填序号)。
(2)配制该溶液时,需要NaCl固体________g。
(3)量取溶剂时,采用仰视的方法读数,会导致所配溶液的溶质质量分数________(填“偏大”“偏小”或“无影响”)。
(4)将配好的溶液稀释成溶质质量分数为5%的NaCl溶液,需加入________g水。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取100g一定质量分数的Ba(OH)2溶液于烧杯中,逐渐加入质量分数为20%的H2SO4溶液.实验过程中,溶液的pH与加入H2SO4溶液的质量关系如图所示.
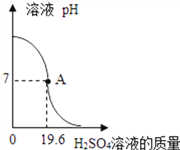
(1)Ba(OH)2中钡元素的质量分数为________,当加入9.8gH2SO4溶液时,溶液的pH________(填“大于”“小于”或“等于”)7
(2)计算Ba(OH)2溶液中溶质的质量分数为________(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com