
【题目】如图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸铜、碳酸钠中的一种,连线两端的物质间能发生化学反应,甲与戊反应产生的气体能使澄清石灰水变浑浊,丙溶液为蓝色,下列能代替图中丁物质的是( ) 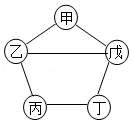
A.Ag
B.BaCl2
C.NaOH
D.CuO
【答案】C
【解析】解:丙溶液呈蓝色,则丙是硫酸铜;甲与戊反应产生的气体能使澄清石灰水变浑浊,则产生的气体是二氧化碳,能反应生成二氧化碳的物质是盐酸和碳酸钠,故甲和戊是盐酸和碳酸钠中的一种;乙既能和碳酸钠也能与盐酸反应,故乙是氢氧化钙;丁是铁,铁能与盐酸反应,故戊是盐酸,甲是碳酸钠;通过推导可知,丙是硫酸铜,戊是盐酸,分析所给选项,只有氢氧化钠既会与盐酸反应,也会与硫酸铜溶液反应,所以能替代丁物质的是NaOH. 故选C.
根据已有的知识进行分析,丙溶液呈蓝色,则丙是硫酸铜;甲与戊反应产生的气体能使澄清石灰水变浑浊,则产生的气体是二氧化碳,能反应生成二氧化碳的物质是盐酸和碳酸钠,故甲和戊是盐酸和碳酸钠中的一种;乙既能和碳酸钠也能与盐酸反应,故乙是氢氧化钙;丁是铁,铁能与盐酸反应,故戊是盐酸,甲是碳酸钠,据此解答.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:初中化学 来源: 题型:
【题目】如图为实验室常用的实验装置,请回答问题: 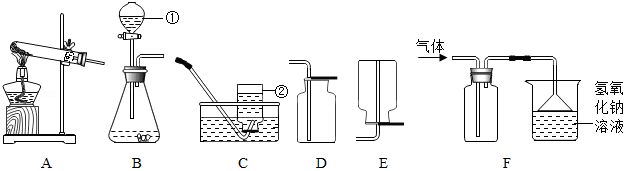
(1)写出带有标号仪器的名称:①;② .
(2)若用A、C装置组合制取氧气,实验中,观察到水槽中气泡(填“刚一冒出”或“连续均匀冒出”)时,开始收集.收集完毕时,应先(填“熄灭酒精灯”或“从水中取出导气管”).
(3)写出用B、E装置组合制取某气体的化学反应方程式: .
(4)硫化氢是有毒气体,能溶于水形成氢硫酸(其化学性质与盐酸相似).常用块状硫化亚铁(FeS)和稀硫酸在常温下发生复分解反应制H2S,某同学用F装置来处理H2S. ①实验室制取H2S的化学方程式为 .
②该装置用于收集H2S,说明其密度比空气(填“大”或“小”).
③用化学方程式表示氢氧化钠溶液的作用是 , 漏斗的作用是
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有溶解度曲线如图,下列有关说法正确的是( ) 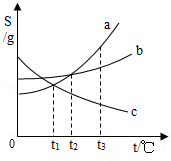
A.t2℃时a、c 两物质溶解度相等
B.将c的不饱和溶液降温可以转化为饱和溶液
C.t1℃时a、c饱和溶液的溶质质量分数相等
D.将t3℃的a、b、c 三种物质的饱和溶液冷却到t1 时,a物质析出最多,无c物质析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(1)探究稀硫酸与氢氧化钠溶液的反应: 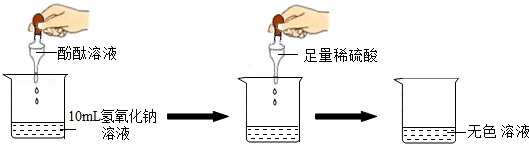
当滴入几滴酚酞试液后,溶液由无色变为色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为: .
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量: 根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是(填“方案一”或“方案二”)
另外一个实验方案错误的原因是;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是 , 实验现象及结论是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】大致测定某溶液是酸性还是碱性,要采取( )
①石蕊试液 ②酚酞试液 ③石蕊试纸 ④pH试纸.
A.只有①②
B.只有①②③
C.只有①④
D.以上都可以
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验: 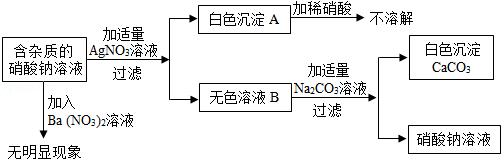 下列判断正确的是( )
下列判断正确的是( )
A.无色溶液B的溶质是硝酸钙
B.原溶液中的杂质一定是氯化钙
C.原溶液中的杂质可能由三种物质组成
D.该实验中涉及的基本反应类型不止一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究: 
【查得资料】(1)该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生.(2)饱和碳酸氢钠溶液不吸收二氧化碳.
【设计实验】小组同学设计了如图所示装置(图中夹持仪器略去) 测定牙膏样品中碳酸钙的含量.
依据图示回答下列问题:
(1)该装置中氢氧化钠溶液的作用是 .
(2)C中观察到有沉淀产生,反应的化学方程式为 .
(3)实验过程中需持续缓缓通入空气,其作用有 .
(4)【解释与结论】实验测得如表数据:
实验次数 | 样品质量(g) | 所用盐酸质量(g) | 所得沉淀质量(g) |
第一次 | 8.00 | 50 | 1.95 |
第二次 | 8.00 | 50 | 1.98 |
第三次 | 8.00 | 50 | 1.96 |
欲计算样品中碳酸钙的含量,应选择的数据是 .
(5)【反思与评价】 1)有人认为不必测定C中沉淀的质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是 .
2)反思实验过程,小刚同学提出应采取必要措施,提高测定准确度.他提出的下列各项措施中,不能提高测定准确度的是(填字母序号).
a.在加入盐酸之前,排净装置内的CO2气体
b.放慢滴加盐酸的速度
c.在A﹣B之间增添盛有浓硫酸的洗气装置
d.在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】白色固体甲可能含有硫酸钠、氢氧化钠、碳酸钠、氯化钠中的一种或几种;无色溶液乙可能含有硝酸钡、氯化钾、为探究它们的成分,进行如下实验. 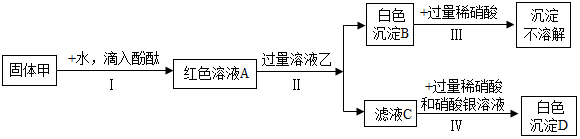
(1)溶液A呈(填“酸性”或“中性”或“碱性”).
(2)固体甲中一定含有的物质是(写化学式).
(3)根据步骤Ⅳ不能确定固体甲中某物质是否存在,其理由是;要确定固体甲中该物质是否存在,需进行的实验操作是 , 观察现象.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com