
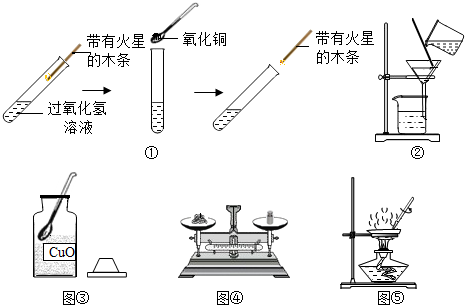
分析 根据催化剂在化学反应前后的化学性质和质量不变以及实验的探究过程进行分析解答即可.
解答 解:过氧化氢在氧化铜的催化作用下分解生成水和氧气,故填:2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑;
(1)图②是过滤操作,玻璃棒起到了引流的作用,把滤出的固体用来重复实验,结果还能加快过氧化氢的分解,说明氧化铜的化学性质反应前后不变,故填:引流;氧化铜在反应前后化学性质不变;
要证明氧化铜的化学性质在化学反应前后不变,可以在不产生气体后的溶液中继续加入过氧化氢溶液,发现仍然能产生气泡即可,故填:在实验①反应完毕后的溶液中继续加入过氧化氢溶液,如果过氧化氢分解产生氧气能使带火星的木条复燃;
过滤得到的氧化铜表面可能有过氧化氢溶液,可以使用蒸馏水清洗,故填:过滤时用蒸馏水洗涤沉涤;
(2)要想证明氧化铜在化学反应前后质量不发生改变,可以将反应后的物质过滤,将过滤得到的固体洗涤烘干后继续称量,故填:③④①②⑤④;
要称量氧化铜的质量,可以先称出滤纸的质量,然后过滤后烘干,将滤纸的质量一同称量,故填:先称出滤纸的质量,过滤后烘干,将滤纸的质量一同称量.
点评 本题考查的是催化剂探究,完成此题,可以依据催化剂的特点以及实验操作方法进行.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:初中化学 来源: 题型:实验探究题
 如图所示,将滴有酚酞的滤纸条放在试管里,如图示放在实验桌上:
如图所示,将滴有酚酞的滤纸条放在试管里,如图示放在实验桌上:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
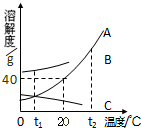 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
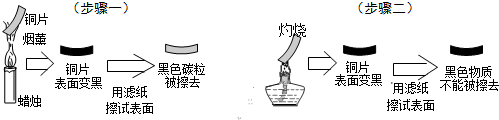
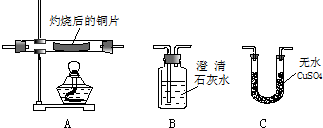
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
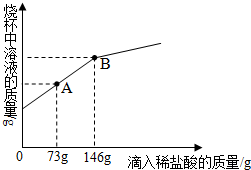 碳酸钙是工业生产的重要原料.烧杯中盛有CaCO3和CaCl2的粉末状混合物42.2g,向其中加入水168.8g后充分搅拌,使混合物中的可溶物完全溶解.然后再向其中逐渐加入溶质的质量分数为10%的稀盐酸,烧杯中不饱和溶液的质量与所加入稀盐酸的质量关系如图所示.请回答下列问题:
碳酸钙是工业生产的重要原料.烧杯中盛有CaCO3和CaCl2的粉末状混合物42.2g,向其中加入水168.8g后充分搅拌,使混合物中的可溶物完全溶解.然后再向其中逐渐加入溶质的质量分数为10%的稀盐酸,烧杯中不饱和溶液的质量与所加入稀盐酸的质量关系如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com