
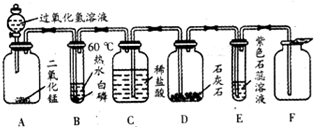
 体积的NaOH溶液,发现塑料瓶变瘪.于是他宣布已验证了CO2与NaOH发生了反应.你认为乙同学的实验结论是否正确?答______,判断的依据是______.
体积的NaOH溶液,发现塑料瓶变瘪.于是他宣布已验证了CO2与NaOH发生了反应.你认为乙同学的实验结论是否正确?答______,判断的依据是______. 2H2O+O2↑;
2H2O+O2↑; 2H2O+O2↑;
2H2O+O2↑;

科目:初中化学 来源: 题型:
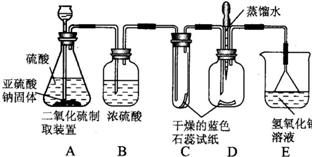 33、二氧化硫(SO2)的含量是空气质量监测的指标之一.二氧化硫易溶于水,二氧化硫跟水在通常情况下能否发生化学反应呢?为探究这个问题,某校兴趣小组的同学利用下图所示的装置进行实验.实验前该小组同学查阅到下列资料内容:①二氧化硫能被浓硫酸干燥;②酸能使湿润的蓝色石蕊试纸变红.
33、二氧化硫(SO2)的含量是空气质量监测的指标之一.二氧化硫易溶于水,二氧化硫跟水在通常情况下能否发生化学反应呢?为探究这个问题,某校兴趣小组的同学利用下图所示的装置进行实验.实验前该小组同学查阅到下列资料内容:①二氧化硫能被浓硫酸干燥;②酸能使湿润的蓝色石蕊试纸变红.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 1 |
| 3 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 河段编号 | 水质类别 | 主要污染指标 | 质量状况 |
| 甲 | Ⅱ | 良好 | |
| 乙 | Ⅳ | 汞 | 一般 |
| 丙 | 劣Ⅴ | 总磷、氮等 | 较差 |
| 宇宙牌化肥--国际首创 主要成分:尿素[CO(NH2)2] 含氮量居全球化肥之首:48% 净含量:50kg/袋 “宇宙”化肥有限责任公司出品 |
查看答案和解析>>
科目:初中化学 来源:课堂三级讲练化学 九年级(上) 题型:059
某校兴趣小组同学在老师的指导下,对居民区附近的一河流(图甲)进行溶解氧的藻类的测定,并根据所测结果绘成图乙,发现AB段溶解氧和藻类大量减少.通过调查,了解到在河流A上游附近有一座酿造厂一将污水直接排放到该河流.请据此回答:

(1)在河流AB段,溶解氧大量减少的主要原因是________________.
(2)D段后,水中的溶解氧和藻类基本恢复,说明该河流生态系统肯定有________________________.
(3)对此污染问题的处理,请你提出一条合理化建议:________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com