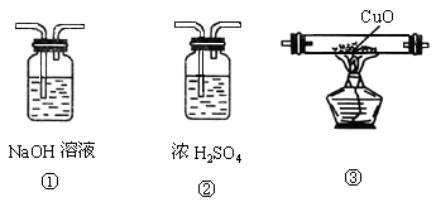
29、实验室用锌粒和稀硫酸反应制取的氢气,经过净化干燥后,还原氧化铜.
(1)根据所得到铜粉的质量,可求得参加反应的氢气的质量,进而计算出应消耗的锌粒和稀硫酸的质量.但实际耗用的锌粒(不含杂质)和稀硫酸的质量都远远超过理论值.从实验过程看,可能的原因有哪些?(至少答出三点原因) ①
氧化铜加热前要先通氢气,排去试管内空气
②
反应后热铜粉还需在氢气中冷却
③
部分氢气通过装有氧化铜的试管时,未与氧化铜反应
(2)Cu
+在酸性溶液中不稳定,可发生反应生成Cu
2+和Cu.Cu与强氧化性酸反应可得到铜盐溶液.现有浓硫酸、浓硝酸、稀硫酸、稀硝酸,而没有其他试剂.Cu
2O是一种红色固体,如何用最简便的实验方法来检验经氢气还原CuO所得到的红色产物中是否含有Cu
2O.
取红色固体少量于试管中,向试管中滴加稀硫酸,充分振荡,若发现溶液变为蓝色,则说明样品中混有Cu2O,若没有发现溶液变为蓝色,则说明样品中没有Cu2O
.

 名校课堂系列答案
名校课堂系列答案