
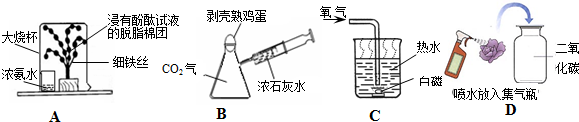
分析 (1)浓氨水具挥发性,氨气极易溶于水,其水溶液显碱性,碱液能使无色的酚酞变色;
(2)二氧化碳能与氢氧化钙反应,使瓶中压强减小;
(3)分析可燃物着火燃烧的条件及白磷燃烧的化学方程式;
(4)酸能使紫色的石蕊变红色.
解答 解:(1)浓氨水具挥发性,也是氨分子不断运动的结果,氨气极易溶于水,其水溶液显碱性,碱液能使无色的酚酞变红色;
(2)二氧化碳气体能和浓氢氧化钙溶液反应,装置内气压减小,外界大气压将熟鸡蛋“吞”入瓶中,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)图示白磷在获得氧气的情况下能燃烧,其化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(4)图D所示实验观察到紫色小花变为红色,是因为CO2+H2O=H2CO3,碳酸能使紫色的石蕊试液变红色.
故答案为:(1)红,B,
(2)Ca(OH)2+CO2═CaCO3↓+H2O;
(3)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(4)CO2+H2O=H2CO3.
点评 本题考查了常见物质的性质,完成此题,可以依据已有的知识进行.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl═AlCl3+3H2O 复分解反应 | |
| B. | 拉瓦锡研究空气成分 2Hg0$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+02 分解反应 | |
| C. | 石笋、石柱形成的原因 CaCO3+CO2+H2O═Ca(HCO3)2 化合反应 | |
| D. | 验证铜和铝的活动性 3Cu+A12(S04)3═3CuS04+2Al 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应都不需要加热 | B. | 所需仪器相同 | ||
| C. | 均可用二氧化锰作催化剂 | D. | 都利用向下排空气法收集氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分别通入澄清石灰水 | B. | 分别通入紫色石蕊试液 | ||
| C. | 分别伸入燃着的木条 | D. | 分别伸入带火星的木条 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 氯化铵与消石灰混合研磨产生氨气:2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H20 | |
| B. | 化工厂用氨、二氧化碳和水制碳酸氢铵:NH3+H2O+C02═NH4HC03 | |
| C. | 氢化钙(CaH2)与水反应可以得到氢气:CaH2+2H20═Ca(OH)2+2H2↑ | |
| D. | 工业合成氨3H2+N2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
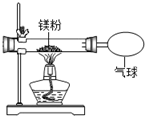 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.| 实验操作 | 实验现象及结论 |
| 实验序号 | 实验1 | 实验2 | 实验3 | / |
| 与镁条反应的溶液 | NH4Cl | NaCl | Na2SO4l | H2O |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后,实验现象 | 气泡明显增多可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com