
科目: 来源:2017届上海市普陀区九年级4月质量调研(二模)化学试卷(解析版) 题型:选择填充题
某粗盐主要成分是NaCl,可能还有Na2CO3、Na2SO4,为检验所含杂质的成分,进行了如下实验:
取少量样品,加水溶解 | 滴入稀盐酸 | 继续滴入氯化钡 | |
实验过程 |
|
|
|
实验现象 | 全部溶解 | 有气泡产生 |
根据实验过程,预测最后的实验现象,且对Na2SO4判断均正确的是
A. 有白色沉淀生成,一定有Na2SO4
B. 先没有沉淀,后有白色沉淀生成,可能含有Na2SO4
C. 无白色沉淀生成,一定没有Na2SO4
D. 无论有无白色沉淀生成,均可能有Na2SO4
查看答案和解析>>
科目: 来源:2017届上海市普陀区九年级4月质量调研(二模)化学试卷(解析版) 题型:信息分析题
查阅资料可以了解元素的某些信息。如图是元素周期表中的一部分。

①该图表示的是硅元素,它的元素符号是_____,硅元素属于______(填写“金属”或“非金属”)元素。
②水晶的成分是二氧化硅(SiO2,其中硅的原子量是28),则水晶的摩尔质量是_________,其中含硅元素的质量分数是___________。
③硅是半导体的主要材料。工业上,通常是在电炉中由碳还原二氧化硅而制得。化学方程式:SiO2 + 2C  Si + 2CO↑ 这样制得的硅纯度约为98%。该反应利用了碳的______(填写“氧化性”或“还原性”),反应过程中回收CO可以避免污染,回收的CO可以用作______________。
Si + 2CO↑ 这样制得的硅纯度约为98%。该反应利用了碳的______(填写“氧化性”或“还原性”),反应过程中回收CO可以避免污染,回收的CO可以用作______________。
查看答案和解析>>
科目: 来源:2017届上海市普陀区九年级4月质量调研(二模)化学试卷(解析版) 题型:信息分析题
如图是浓盐酸试剂瓶上标签的部分内容。请回答:

①该浓盐酸的溶质是____(填化学式);打开浓盐酸的瓶盖看到的现象是___________________。
②现要配制3%的稀盐酸120g,需要这种浓盐酸_______g;
③盐酸属于无氧酸,分类的依据是____________________;
④盐酸具有酸的通性。有盐酸参加的中和反应的化学方程式______________(任写一个);实验室通常检验盐酸中含有氯元素的化学方程式_________________。
查看答案和解析>>
科目: 来源:2017届上海市普陀区九年级4月质量调研(二模)化学试卷(解析版) 题型:信息分析题
“侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱。
NaCl和NH4Cl的溶解度表:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度 (g/100g水) | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
请根据提供的信息,回答问题:
①10℃时,NaCl的溶解度是______;
②如 图中,表示NH4Cl的溶解度曲线是_______(填“A”或“B”)。

③常温20℃时,配制的饱和食盐水的质量分数为_____,将食盐水的温度提高,溶液中溶质的质量分数也将提高,而实际生产中往往在常温下进行,这样做的理由是____________________;
④若NaCl和NH4Cl溶液溶质质量分数相同,表示其溶NaCl和NH4Cl的溶解度曲线图液状态的点在右图中可能位于的区域是_______(选填I、II、III、IV);
⑤生产中通入氨气及二氧化碳,若要提高这些气体的溶解度,下列做法可行的是______(选填编号)。
A.增大压强 B.升高温度 C.增加水量
查看答案和解析>>
科目: 来源:2017届上海市普陀区九年级4月质量调研(二模)化学试卷(解析版) 题型:信息分析题
为证明水中含有氢元素,有多种实验方法可行。
①电解水的实验可证明水中含有氢元素,该反应的化学方程式是________________;请再列举一种实验方法__________________(下列②中方法除外)。
②实验室也可以利用氢气还原氧化铜的方法,装置如下图所示(图中浓硫酸起干燥作用):

“A”中盛放锌和稀硫酸的玻璃仪器名称是_____。根据________现象,就可以判断有水生成,进一步得出水中有氢元素。
③“C”中如果有8 g氧化铜参加反应,理论上可以得到的水有多少g?含有水分子有多少个?(请根据化学方程式列式计算)______________
④实验完毕,装置中药品的质量一定减轻的是_______(选填上图装置编号:A、B、C、D、E)。
有机物中一定含有____(填写元素名称),许多有机物中也同样含有氢元素。为证明甲烷中含有氢元素,回答相关问题:
⑤如果进行如图实验,通过燃烧证明有氢元素,该实验方法中看到的现象是______________。

⑥如果进行分解实验,只要证明有______单质生成,也可证明甲烷中有氢元素。
查看答案和解析>>
科目: 来源:2017届上海市普陀区九年级4月质量调研(二模)化学试卷(解析版) 题型:信息分析题
下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图。

①试剂I的名称为________;操作Y为过滤,所用到的玻璃仪器有___种,过滤后滤液仍有浑浊,而过滤器完好,则可能操作不当引起,该操作可能是___________。
②硫酸与铁反应的化学方程式为____________________________;
硫酸与氧化铁反应的化学方程式___________________________;
往铁粉(含少量氧化铁)中加入硫酸,除铁、氧化铁与硫酸发生反应外,一定还发生其它反应。作出这种判断的依据是________________________________。
③氢氧化亚铁转变成氢氧化铁的反应为:4Fe(OH)2+O2+xH2O→4Fe(OH)3,经配平后,x为____。
④最后将Fe(OH)3进行一定处理成为Fe3O4。如果取用某种铁粉(含少量氧化铁)样品进行实验室模拟,若该样品含铁元素16.8g,最后得到Fe3O4_______mol。
查看答案和解析>>
科目: 来源:2017届广东省清远市九年级中考一模化学试卷(解析版) 题型:选择填充题
下列过程是通过物理变化获得能量的是
A. 风力发电 B. 煤燃烧发电
C. 烧火取暖 D. 汽油燃烧驱动汽车
查看答案和解析>>
科目: 来源:2017届广东省清远市九年级中考一模化学试卷(解析版) 题型:选择填充题
下列有关物质的化学式、名称、俗名、分类不完全对应的是
A. NaCl 氯化钠 食盐 盐类 B. CaO 氧化钙 熟石灰 氧化物
C. Na2CO3 碳酸钠 纯碱 盐类 D. NaOH 氢氧化钠 烧碱 碱类
查看答案和解析>>
科目: 来源:2017届广东省清远市九年级中考一模化学试卷(解析版) 题型:选择填充题
遵守实验室规则,学习基本的实验操作方法,是实验成功的重要保证.下列实验操作正确的是
A. 检查装置的气密性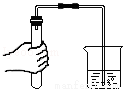
B. 稀释浓硫酸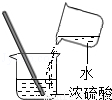
C. 气体验满
D. 加热液体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com