
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示。下列有关说法正确的是
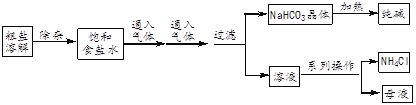
A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
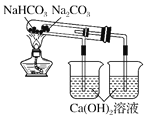
D. 如图所示装置可以比较Na2CO3和NaHCO3晶体热稳定性
【答案】C
【解析】A、除去粗盐中的钙离子、镁离子、硫酸根离子及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠除去钙离子和过量的钡离子,盐酸要放在最后,来除去过量的碳酸钠和氢氧化钠,选项A错误;B、二氧化碳在水中溶解度较小,氨气溶解度较大,故应先通入氨气,碱性溶液中再通入二氧化碳,二氧化碳的溶解度增大,可以达到实验目的,选项B错误;C、从溶液中得到固体,需要加热浓缩、冷却结晶、过滤等操作,这些过程中需要玻璃棒搅拌、引流等,选项C正确;D、碳酸钠加热不易分解,碳酸氢钠加热容易分解,故小试管中盛放碳酸氢钠,大试管盛放碳酸钠,碳酸氢钠间接加热能分解,碳酸钠直接加热不分解,能证明两者的稳定性,图中放反了,选项D错误。答案选C。


科目:高中化学 来源: 题型:
【题目】已知:P4(白磷,s)+5O2(g)═P4O10(s)△H=﹣2983.2kJ/mol,
P(红磷,s)+ ![]() O2(g)═
O2(g)═ ![]() P4O10(s)△H=﹣738.5kJ/mol.
P4O10(s)△H=﹣738.5kJ/mol.
试写出白磷转化为红磷的热化学方程式;
相同状况下,能量较低的是 , 白磷的稳定性于红磷(填“高”或“低”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法不正确的是( )
A.氯乙烯分子中所有原子共平面B.乙醇、乙酸都能发生取代反应
C.乙酸乙酯、甲酸丙酯的密度都小于水D.淀粉和纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=-1200KJ/mol,温度不同(T2>T1)其他条件相同时,下列图像正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者小于后者的是
①C(s)+ ![]() O2(g) ===CO(g);ΔH1 C(s)+O2(g) ===CO2(g);ΔH2
O2(g) ===CO(g);ΔH1 C(s)+O2(g) ===CO2(g);ΔH2
②S(g)+O2(g) ===SO2(g);ΔH3 S(s)+O2(g) ===SO2(g);ΔH4
③CaO(s)+H2O(l) ===Ca(OH)2(s);ΔH5 CaCO3(s) ===CaO(s)+CO2(g);ΔH6
A.② B.①② C.①③ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4 , 从而得到纯净的NaNO3溶液.相应的实验过程可用如图表示:
(1)写出下列物质的化学式X、A、B
(2)上述实验流程中加入过量的Na2CO3的目的是 .
(3)按此实验方案得到的溶液3中肯定含有(填化学式)杂质;为了解决这个问题,可以向溶液3中加入过量的(填化学式),之后若要获得固体NaNO3需进行的实验操作是(填操作名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度均为 0.1 molL-1、体积均为 100 mL 的两种一元酸 HX、HY的溶液中,分别加入 NaOH固体,lg[c(H+ )/c(OH- )]随加入 NaOH的物质的量的变化如图所示。下列说法正确的是
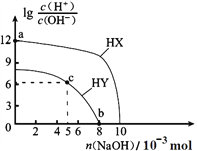
A. 常温下电离常数:HX < HY![]()
B. a 点由水电离出的 c(H+)=10-12 molL-1
C. c 点溶液中:c(Y- )>c(HY )![]()
D. b 点时酸碱恰好完全中和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com