
某有机物X(C13H13O7Br)遇到FeCl3溶液显紫色,其部分结构简式如下:

已知:①X在足量的氢氧化钠水溶液中加热,可以得到A、B、C三种有机物;
②室温下B经盐酸酸化可以得到苹果酸D,D的分子式为C4H6O5;
③C能发生银镜反应。
试回答:
(1)D中所含官能团的名称是 ,D不能发生的反应类型是(填序号) 。
①加成反应,②消去反应,③氧化反应,④酯化反应。
(2)D的一种同分异构体E有如下特 点:lmol E可以和3mol金属钠发生反应,放出33.6LH2(标准状况下),lmolE可以和足量NaHCO3溶液反应,生成lmolCO2,lmolE还可以发生银镜反应,生成2molAg。试写出E可能的结构简式 。
点:lmol E可以和3mol金属钠发生反应,放出33.6LH2(标准状况下),lmolE可以和足量NaHCO3溶液反应,生成lmolCO2,lmolE还可以发生银镜反应,生成2molAg。试写出E可能的结构简式 。
(3)A和D在一定条件下可以生成八元环酯,写出此反应的化学方程式 。
(4)若C经盐酸酸化后得到的有机物F,其苯环上的一溴代物只有两种,则F可能的结构简式为 ,写出其中任意一种和银氨溶液发生反应的化学方程式 。
(5)F的一种同分异构体是制取阿司匹林( )的原料,试写出其结构简式 ,它在一定条件下生成高分子化合物的方程式为 。
)的原料,试写出其结构简式 ,它在一定条件下生成高分子化合物的方程式为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届湖北省襄阳市四校高三上学期期中化学试卷(解析版) 题型:选择题
下列实验对应的现象及结论均正确且两者具有因果关系的选项是( )
选项 | 实验 | 现象 | 结论 |
A | SO2通入BaCl2溶液,然后滴入稀硝酸 | 有白色沉淀,白色沉淀不溶于稀硝酸 | 所得沉淀为BaSO3,后转化为BaSO4 |
B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
C | 将稀硫酸滴入碳酸钠溶液中产生的气体通入硅酸钠溶液 | 有白色沉淀生成 | 证明非金属性S>C>Si |
D | 向含有淀粉的FEI2溶液中滴加足量的氯水 | 溶液变蓝 | 还原性:I->FE2+ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:选择题
已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液形成无色溶液,其化学方程式是PbSO4+2NH4Ac=Pb(Ac)2+(NH4)2SO4。当在Pb(Ac)2(醋酸铅)溶液中通入H2S时,有黑色沉淀PbS生成。表示这个反应的有关离子方程式正确的是
A.Pb(Ac)2+H2S=PbS↓+2HAc
B.Pb2++H2S=PbS↓+2H+
C.Pb2++2Ac-+H2S=PbS↓+2HAc
D.Pb2++2Ac-+2H++S2-=PbS↓+2HAc
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上期中化学试卷(解析版) 题型:实验题
直接排放含SO2的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关SO2性质的探究活动。
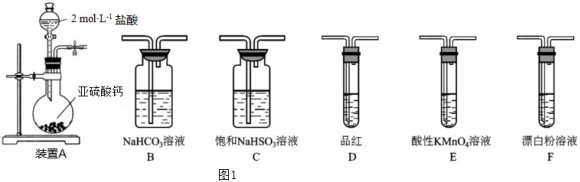
(1)装置A中反应的离子方程式为 。
(2)选用图1以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是 。
②丙同学设计的合理实验方案为:按照A→C →尾气处理(填字母)顺序连接装置。其中装置C的作用是 。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是 。

(3)利用如图2的装置A测残液中SO2的含量。量取10.00 mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00 mL 0.1000 mol/L的KMnO4标准溶液吸收。充分反应后,再用0.2000 mol/L的KI溶液滴定过量的KMnO4,消耗KI溶液25.00 mL。
(已知:5SO2+2MnO4-+2H2O==2Mn2++5SO42-+4H+,10I-+2MnO4-+16H+==2Mn2++5I2+8H2O)
①该装置中仪器C的名称为 ,水通入C的进口为_____________。
②残液中SO2的含量为 mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上期中化学试卷(解析版) 题型:选择题
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是

甲 | 乙 | 丙 | 戊 | |
① | SiO2 | NaOH | Na2SiO3 | CO2 |
② | Fe | H2O | Fe2O3 | H2 |
③ | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
④ | Na2O2 | CO2 | O2 | Na |
A.①③ B.①② C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三11月模拟化学卷(解析版) 题型:选择题
某有机物X(C4H6O5)广泛存在于许多水果内,尤其以苹果、葡萄、西瓜、山楂内为多。该化合物具有如下性质:①1 molX与足量金属钠反应产生1.5 mol气体;②在有浓H2SO4和加热条件下,X与醇或羧酸均反应生成有香味的产物;③X在一定条件下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应。根据上述信息,对X的结构判断正确的是
A.X中含有碳碳双键 B.X中含有三个羟基和一个-COOR
C.X中含有一个羧基和两个羟基 D.X中含有两个羧基和一个羟基
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三11月模拟化学卷(解析版) 题型:选择题
用下图所示装置检验乙烯时不需要除杂的是( )
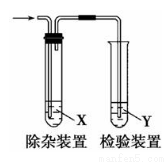
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | C2H5OH与浓H2SO4加热至170 ℃ | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓H2SO4加热至170 ℃ | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三月考二化学试卷(解析版) 题型:填空题
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。第三代太阳能电池就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池及薄膜Si系太阳能电池。
(1)现代化学中,常利用 上的特征谱线来鉴定元素
(2)铟是镓的同主族的相邻元素,它位于元素周期表的 区,它的价电子排布式是 。
(3)硒为第4周期氧族元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为 。(用元素符号表示)
(4)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有特殊的性质。如BF3与一定量水能形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:

①晶体Q中各种微粒间的作用力不涉及 (填序号)
A离子键 B共价键 C配位键 D金属键 e氢键 f范德华力
②R中阳离子的空间构型为 ,阴离子的中心原子轨道采用 杂化

(5)一种铜金合金晶体如图所示(Au原子位于顶点,Cu原子位于面心),则该合金中Au原子与Cu原子个数之比为__________,若该晶胞的边长为a pm,则合金的密度为___________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北石家庄一中高二上期中考试化学试卷(解析版) 题型:填空题
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ/mol
N2(g)+3H2(g) 2NH3(g);△H=﹣92.4kJ/mol
2NH3(g);△H=﹣92.4kJ/mol
2H2(g)+O2(g)=2H2O(g);△H=﹣483.6kJ/mol
写出氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为。
(2)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2。

写出石墨I电极上发生反应的电极反应式 ;
在电解池中生成N2O5的电极反应式为 。
(3)以甲醇燃料电池为电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2molCH3OH,阴极产生标况下气体的体积为 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com