
已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液形成无色溶液,其化学方程式是PbSO4+2NH4Ac=Pb(Ac)2+(NH4)2SO4。当在Pb(Ac)2(醋酸铅)溶液中通入H2S时,有黑色沉淀PbS生成。表示这个反应的有关离子方程式正确的是
A.Pb(Ac)2+H2S=PbS↓+2HAc
B.Pb2++H2S=PbS↓+2H+
C.Pb2++2Ac-+H2S=PbS↓+2HAc
D.Pb2++2Ac-+2H++S2-=PbS↓+2HAc
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:填空题
(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;
FeO(s)+CO(g) ΔH1,平衡常数为K1;
反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2。
FeO(s)+H2(g) ΔH2,平衡常数为K2。
在不同温度时K1、K2的值如下表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
①反应 CO2(g) + H2(g) CO(g) + H2O(g) ΔH,平衡常数K,则ΔH = (用ΔH1和ΔH2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g)
CO(g) + H2O(g) ΔH,平衡常数K,则ΔH = (用ΔH1和ΔH2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g) CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH > 0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) ΔH > 0,CO2的浓度与时间的关系如图所示:
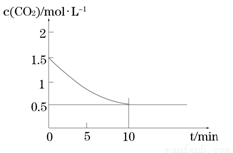
① 该条件下反应的平衡常数为 ;
② 下列措施中能使平衡时 增大的是 (填序号)
增大的是 (填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③ 一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母)。
a.容器中压强不变
b.气体的密度不再改变
c.v正(CO2)=v逆(CO)
d.c(CO2)=c(CO)
e.容器内气体总物质的量不变
查看答案和解析>>
科目:高中化学 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:推断题
[化学——选修5:有机化学基础]
已知一个碳原子上连有两个羟基时,易发生下列转化:
请根据下图回答问题:

(1)E中含 有官能团的名称是 ;③的反应类型是 ,C跟新制的氢氧化铜反应的化学方程化为 。
有官能团的名称是 ;③的反应类型是 ,C跟新制的氢氧化铜反应的化学方程化为 。
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1,则B的分子式为 ,F的分子式为 。
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀0.11mm线宽芯片的关键技术.F是这种高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③芳环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应.G可能有
种结构,写出它们的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2017届广东省惠州市高三上学期调研一化学试卷(解析版) 题型:选择题
25℃时,0.1 mol/L下列溶液的pH如下表,有关比较正确的是
序号 | ① | ② | ③ | ④ | ⑤ |
溶液 | NaCl | CH3COONH4 | NaClO | NaHCO3 | Na2CO3 |
pH | 7.0 | 7.0 | 10.3 | 8.3 | 11.6 |
A.酸性的相对强弱:HClO<HCO3-
B.由水电离产生的c(H+):① = ②
C.溶液③④中酸根离子浓度:c(ClO-)>c(HCO3-)
D.在④⑤溶液等体积混合后的溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:计算题
将50g密度ρ=0.98g/mL的10%的氨水和100g密度ρ=0.93g/mL的40%的氨水混合,得到ρ=0.95g/mL氨水溶液,求所得氨水的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:选择题
电解质溶于水后电离出的阴、阳离子是能够导电的,而且溶液的导电能力与溶液中离子所带的电荷的浓度有关,下列溶液的导电能力最强的是
A.0.2mol.L-1NaCl溶液
B.0.15mol.L-1MgCl2溶液
C.0.2mol.L-1BaCl2溶液
D.0.25mol.L-1HCl溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:选择题
下列实验能达到测量要求的是
A. 用托盘天平称取35.20gNaOH
B. 用10mL量筒量取8.50mL浓盐酸配一定物质的量浓度溶液
C. 用25ml滴定管量取15.80ml浓溶液配一定物质的量浓度溶液
D. 用pH试纸测得溶液pH为4.2
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三11月模拟化学卷(解析版) 题型:推断题
某有机物X(C13H13O7Br)遇到FeCl3溶液显紫色,其部分结构简式如下:

已知:①X在足量的氢氧化钠水溶液中加热,可以得到A、B、C三种有机物;
②室温下B经盐酸酸化可以得到苹果酸D,D的分子式为C4H6O5;
③C能发生银镜反应。
试回答:
(1)D中所含官能团的名称是 ,D不能发生的反应类型是(填序号) 。
①加成反应,②消去反应,③氧化反应,④酯化反应。
(2)D的一种同分异构体E有如下特 点:lmol E可以和3mol金属钠发生反应,放出33.6LH2(标准状况下),lmolE可以和足量NaHCO3溶液反应,生成lmolCO2,lmolE还可以发生银镜反应,生成2molAg。试写出E可能的结构简式 。
点:lmol E可以和3mol金属钠发生反应,放出33.6LH2(标准状况下),lmolE可以和足量NaHCO3溶液反应,生成lmolCO2,lmolE还可以发生银镜反应,生成2molAg。试写出E可能的结构简式 。
(3)A和D在一定条件下可以生成八元环酯,写出此反应的化学方程式 。
(4)若C经盐酸酸化后得到的有机物F,其苯环上的一溴代物只有两种,则F可能的结构简式为 ,写出其中任意一种和银氨溶液发生反应的化学方程式 。
(5)F的一种同分异构体是制取阿司匹林( )的原料,试写出其结构简式 ,它在一定条件下生成高分子化合物的方程式为 。
)的原料,试写出其结构简式 ,它在一定条件下生成高分子化合物的方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江双鸭山一中高一上期中考试化学试卷(解析版) 题型:填空题
碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)该反应还原产物与氧化产物质量比是;
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的苯,振荡,观察到的现象是___________________________;
(3)某学生在一次分液操作中发现上下层溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断方法_________。
(4)在容量瓶的使用方法中,下列操作正确的是____________;
A.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1-2cm处,用胶头滴管加蒸馏水至刻度线。
B.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
C.使用容量瓶前检验是否漏水
D.容量瓶用水洗净后,再用待配溶液洗涤
(5)用容量瓶配制一定物质的量浓度的稀硫酸,下面操作造成所配稀硫酸溶液浓度偏高的是______
A.转移时没有洗涤烧杯、玻璃棒
B.溶解的时候溶液没有冷却到室温就转移
C.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.向容量瓶加水定容时眼睛俯视液面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com