
���� X��Y��Z��Ϊ������Ԫ�أ�ԭ��������������X�ĵ���Ϊ�ܶ���С�����壬��XΪHԪ�أ�Yԭ������������������������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����YΪOԪ�أ�Z��Xԭ��������������ͬ������ͬ���ڣ�Z��ԭ����������������ZΪNa���ݴ˽��
��� �⣺X��Y��Z��Ϊ������Ԫ�أ�ԭ��������������X�ĵ���Ϊ�ܶ���С�����壬��XΪHԪ�أ�Yԭ������������������������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����YΪOԪ�أ�Z��Xԭ��������������ͬ������ͬ���ڣ�Z��ԭ����������������ZΪNa��
��1��������������֪��XΪ�⡢YΪ����ZΪ�ƣ��ʴ�Ϊ���⣻�����ƣ�
��2��������Ԫ����ɵĻ������У��Ⱥ��й��ۼ��ֺ������Ӽ�����NaOH��Na2O2���ʴ�Ϊ��NaOH��Na2O2��
��3��X��Y��ɵĻ������У��Ⱥ��м��Թ��ۼ��ֺ��зǼ��Թ��ۼ�����H2O2���������������������������ط�Ӧ�����ӷ���ʽΪ��5H2O2+2MnO4-+6H-=2Mn2++8H2O+5O2�����˻����ﻹ�ɽ����Թ�ҵ��ˮ�е�CN-����Ϊ̼���κͰ�����Ӧ�����ӷ���ʽΪ��H2O2+CN-+OH-=CO32-+NH3��
�ʴ�Ϊ��H2O2��5H2O2+2MnO4-+6H-=2Mn2++8H2O+5O2����H2O2+CN-+OH-=CO32-+NH3��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��Ƚϻ�����ּ�ڿ���ѧ���Ի���֪ʶ���������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ ����� | B�� | ������ ���� | C�� | ��Һ ��Һ | D�� | ��Һ ��ɢϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
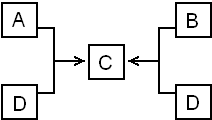 ��֪A�����ᷴӦ����B��������������ͼ�ش��������⣺
��֪A�����ᷴӦ����B��������������ͼ�ش��������⣺ ��C�Ļ�ѧʽΪNaAlO2��B+D��C�����ӷ���ʽΪAl3++4OH-=2AlO2-+2H2O��
��C�Ļ�ѧʽΪNaAlO2��B+D��C�����ӷ���ʽΪAl3++4OH-=2AlO2-+2H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ƿ���������ɫ���� | B�� | ����ƿ���л��dz��� | ||
| C�� | ����ƿ�ڱ�������״Һ����� | D�� | ����ƿ�����ػ�ɫ�̳��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ȼ�������Һ��ͨ��������Fe2++Cl2=Fe3++2Cl- | |
| B�� | ������ͨ���������������Һ�У�Cl2+2OH-=Cl-+ClO-+H2O | |
| C�� | ��Ƭ������������Һ��Ӧ��Al+2OH-=AlO2-+H2�� | |
| D�� | NaHCO3��Һ�м������CO32-+2H+=H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ࡢ��֬�������ʶ�����C��H��O����Ԫ����ɵ� | |
| B�� | ���ࡢ��֬�������ʶ��Ǹ߷��ӻ����� | |
| C�� | ���ࡢ��֬�������ʶ��ܷ���ˮ�ⷴӦ | |
| D�� | ��֬���ͺ�֬��֮�֣����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���� T/��n/mol | NO | CO | E | F |
| ��ʼ | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ����CuSO4��Һ | C�� | ���뱥��ʳ��ˮ | D�� | ��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com