
【题目】热催化合成氨面临的两难问题是:釆用高温增大反应速率的同时会因平衡限制导致NH3产率降低。我国科研人员研制了TiHFe双温区催化剂(Ti-H区域和Fe区域的温度差可超过100℃)。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是( )
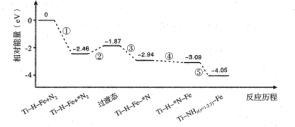
A.①为氮氮三键的断裂过程
B.①②③在低温区发生,④⑤在高温区发生
C.使用Ti-H-Fe双温区催化剂使合成氨反应转变为吸热反应
D.④为N原子由Fe区域向Ti-H区域的传递过程
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 除去乙醇中的少量水,方法是加入新制生石灰,经过滤后即得乙醇
B. HOCH2CH(CH3)2与(CH3)3COH属于碳链异构
C. 除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量烧碱溶液,通过分液即得乙酸乙酯
D. 一个苯环上已经连有-CH3、-CH2CH3、-OH三种基团,如果在苯环上再连接一个-CH3,其同分异构体有16种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10 mL 0.1 mol/L的HR溶液中逐滴滴入0.l mol/L 的氨水,溶液pH及导电性变化如图。
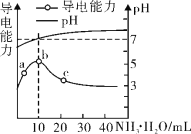
下列分析正确的是
A.HR为强酸
B.加入10 mL 氨水时,溶液中c(NH4+)>c(R-)
C.c点溶液存在c(NH4+)<c( R-)
D.b点的离子浓度大于a点的离子浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息时代产生的电子垃圾处理不当会对环境构成威胁。某研究小组将废弃的线路板处理后,得到含Cu、Al及少量Fe的金属混合物,并设计如下流程制备硫酸铜和硫酸铝晶体。

请回答:
(1)步骤①~③所涉及的实验操作方法中,属于过滤的是______(填序号)。
(2)步骤①中Cu、Al、Fe均能与稀硫酸和浓硝酸的混合物在加热条件下反应,其中氮元素全部转化为NO。该步骤中稀硫酸的作用是______。
(3)下列关于步骤②的说法正确的是______(填字母)。
a 沉淀B为白色固体
b H2O2的作用是将Fe2+氧化为Fe3+
c 可以用Ba(OH)2溶液替换NaOH溶液
(4)已知AlO2-+ 4H+=Al3+ + 2H2O。由沉淀B制取Al2(SO4)3·18H2O的操作是:将沉淀B转移到烧杯中,______,将溶液加热蒸发、冷却结晶、过滤得到产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]比FeSO4稳定,不易被氧气氧化,常用于代替FeSO4作分析试剂。某小组尝试制备少量(NH4)2Fe(SO4)2·6H2O并探究其分解产物。

I.制备硫酸亚铁铵晶体的流程如下:
(1)铁屑溶于稀硫酸的过程中,适当加热的目的是_________。
(2)将滤液转移到_________中,迅速加入饱和硫酸铵溶液,直接加热蒸发混合溶液,观察到_________停止加热。蒸发过程保持溶液呈较强酸性的原因是_________。
Ⅱ.查阅资料可知,硫酸亚铁铵晶体受热主要发生反应:
____(NH4)2Fe(SO4)2·6H2O=____Fe2O3+____SO2↑+____NH3↑+____N2↑+____H2O
但伴有副反应发生,生成少量SO3和O2。设计以下实验探究部分分解产物:
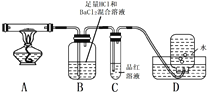
(3)配平上述分解反应的方程式。
(4)加热过程,A中固体逐渐变为_______色。
(5)B中迅速产生少量白色沉淀,反应的离子方程式为______。
(6)C的作用是_________。
(7)D中集气瓶能收集到O2,____ (填“能”或“不能”)用带火星木条检验。
(8)上述反应结来后,继续证明分解产物中含有NH3的方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电化学法生产硫酸的工艺示意图如图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子,已知S(g)在负极发生的反应为可逆反应,则下列说法正确的是( )
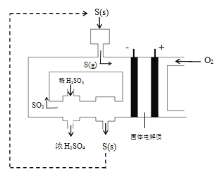
A.在负极S(g)只发生反应S-6e-+3O2-=SO3
B.该工艺用稀硫酸吸收SO3可提高S(g)的转化率
C.每生产1L浓度为98%,密度为1.84g/mL的浓硫酸,理论上将消耗30mol氧气
D.工艺中稀硫酸浓度增大的原因是水参与电极放电质量减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PVAc是一种具有热塑性的树脂,可合成重要的高分子材料![]() ,合成路线如下:
,合成路线如下:
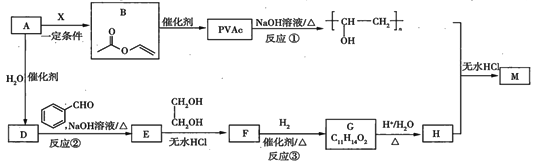
已知:
Ⅰ.![]() ;
;
Ⅱ.RCHO+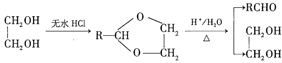
(1)标准状况下,![]() 气态烃
气态烃![]() 的质量是5.2g,则
的质量是5.2g,则![]() 的结构简式为___________。
的结构简式为___________。
(2)已知![]() 为加成反应,则
为加成反应,则![]() 的结构简式为_______;
的结构简式为_______;![]() 中所含官能团的名称是__________。
中所含官能团的名称是__________。
(3)反应①的化学方程式为__________________。
(4)反应③的化学方程式为__________________。
(5)在![]() 的转化过程中,乙二醇的作用是________________。
的转化过程中,乙二醇的作用是________________。
(6)已知![]() 的链节中除苯环外,还含有六元环状结构,则
的链节中除苯环外,还含有六元环状结构,则![]() 的结构简式为____________。
的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在试管中进行下列实验,现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向硫酸铜水溶液中逐滴加入氨水 | 先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液 |
B | 向I2的CCl4溶液中加入浓KI溶液,振荡 | 溶液紫红色变浅 |
C | 向橙色的K2Cr2O7溶液中加入10滴浓硫酸,振荡 | 溶液由橙色变为黄色 |
D | 向饱和硼酸溶液中加入Na2CO3溶液 | 无明显现象 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示。下列说法正确的是( )

A.m=2
B.在Xm-中,硼原子轨道的杂化类型相同
C.1、2原子间和4、5原子间的化学键可能是配位键
D.Xm-中含离子键和配位键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com