
某配位化合物的水溶液为深蓝色,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1.其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n﹣1)d n+6nsl,回答下列问题.
(1)元素D在周期表中的位置是 .
(2)该配位化合物的化学式为 .
(3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 .
(4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 .
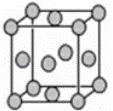
(5)已知E的晶胞结构如下图所示,则E的配位数 ;EDC4常作电镀液,其中DC42﹣的空间构型是 ,其中D原子的杂化轨道类型是 .
考点: 位置结构性质的相互关系应用;配合物的成键情况.
分析: 某配位化合物为深蓝色晶体,由原子序数由小到大的A、B、C、D、E五种元素构成,其原子个数比为14:4:5:1:1.其中C、D元素同主族且原子序数D为C的二倍,则C为O元素、D为S元素;E元素的外围电子排布为(n﹣l)dn+6nsl,则n+6=10,故n=4,故其外围电子排布为3d104sl,则E为Cu;故该深蓝色晶体应含有[Cu(NH3)4]2+、SO42﹣,结合原子序数可知A为H、B为N,由原子数目之比,可知该配合物含有1个结晶水,故其化学式为:[Cu(NH3)4]SO4•H2O,据此进行解答.
解答: 解:某配位化合物为深蓝色晶体,由原子序数由小到大的A、B、C、D、E五种元素构成,其原子个数比为14:4:5:1:1.其中C、D元素同主族且原子序数D为C的二倍,则C为O元素、D为S元素;E元素的外围电子排布为(n﹣l)dn+6nsl,则n+6=10,故n=4,故其外围电子排布为3d104sl,则E为Cu;故该深蓝色晶体应含有[Cu(NH3)4]2+、SO42﹣,结合原子序数可知A为H、B为N,由原子数目之比,可知该配合物含有1个结晶水,故其化学式为:[Cu(NH3)4]SO4•H2O,
(1)D为S元素,其原子序数为16,处于周期表中第三周期ⅥA族,
故答案为:第三周期ⅥA族;
(2)由上述分析可知,该配位化合物的化学式为:[Cu(NH3)4]SO4•H2O,
故答案为:[Cu(NH3)4]SO4•H2O;
(3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,分别为H2O与H2O2,由于H2O与H2O2之间形成氢键,两种化合物可任意比互溶,
故答案为:H2O与H2O2之间形成氢键;
(4)A元素与B元素可形成分子式为H2N2的化合物,该化合物的分子具有平面结构,应存在N=N双键,则其结构式为:H﹣N=N﹣H,
故答案为:H﹣N=N﹣H;
(5)根据晶胞结构可知,该晶胞为面心立方结构,所以铜原子的配位数为12;CuSO4常作电镀液,其中SO42﹣中S原子价层电子对数=4+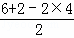 =4,S原子不含孤对电子,故其为正四面体构型,S原子采取sp3杂化,
=4,S原子不含孤对电子,故其为正四面体构型,S原子采取sp3杂化,
故答案为:12;正四面体;sp3杂化.
点评: 本题是对物质结构与性质的考查,题目难度中等,试题涉及元素化合物推断、氢键、结构式、微粒构型判断、杂化轨道、晶胞计算等知识点,解答关键是根据配位化合物为深蓝色晶体进行推断,试题培养了学生的分析、理解能力.


科目:高中化学 来源: 题型:
下列关于油脂的叙述正确的是( )
|
| A. | 油脂有固定的熔、沸点 |
|
| B. | 油脂是高级脂肪酸的甘油酯 |
|
| C. | 油脂都不能使溴的四氯化碳溶液褪色 |
|
| D. | 油脂分成油和脂肪,油的熔点高于脂肪 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2A(g)⇌2B(g)+E(g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是()
A. 加压 B. 减压 C. 减少E的浓度 D. 降温
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙、丁四种金属,把甲、丙浸入稀硫酸中,用导线连接时丙为负极;把乙、丁分别浸入稀硫酸中,丁产生气泡的速率更大;把甲、乙用导线连接浸入稀硫酸中,甲上有气泡冒出;把丙浸入丁的硝酸盐溶液中,丙的表面有丁析出.这四种金属的活动性由强到弱的顺序是.
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是()
A. 60g SiO2中含有NA个SiO2分子
B. 标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2NA
C. 1mol CO2与含1mol NaOH的溶液反应后,溶液中HCO3﹣数为NA
D. 1mol C5H12分子中共价键总数为16NA
查看答案和解析>>
科目:高中化学 来源: 题型:
能在溶液中大量共存的一组离子是 ( )
A . NH4+ 、Ag+ 、PO43-、Cl- B.Fe3+、H+、I-、 HCO3-
C. K+、 Na+、 NO3- 、 MnO4- D.Al3+ 、Mg2+、SO42- 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中化合物的性质比较,不正确的是 ( )
A.酸性:HClO4>HBrO4>HIO4 B.稳定性:PH3>H2S> HCl
C.碱性:NaOH>Mg(OH)2>Al(OH)3 D.非金属性F>O>S
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列事实所列出的相应结论正确的是()
实 验 事 实 结 论
① Cl2的水溶液可以导电 Cl2是电解 质
质
② 将燃烧的镁条放入CO2中能继续燃烧 还原性:Mg>C
③ NaHCO3溶液与Na溶液混合产生白色沉淀 酸性:HCO3﹣>Al(OH)3
④ 常温下白磷可自燃而氮气须在放电时才与氧气反应 非金属性:P>N
⑤ 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 该溶液一定有NH4+
A. ①②③ B. ②③⑤ C. ③④⑤ D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com