
【题目】向10 mL 0.2 mol/L的KIO3溶液中逐渐加入NaHSO3粉末,生成的I2的物质的量随所加NaHSO3的物质的量变化如图所示,下列说法不正确的是( )

A.A点对应的I2的物质的量为1.0×10-3 mol
B.oa : ab = 4 : 1
C.当溶液中的n(I2) = 5×10-4 mol时,加入NaHSO3的物质的量可能为2.5×10-3 mol或5.5×10-3 mol
D.由ab段反应可知,氧化性I2 >![]()
【答案】B
【解析】
加入NaHSO3的物质的量在0→a,发生的反应为:2IO3-+5HSO3-=5SO42-+I2+H2O+3H+,加入NaHSO3的物质的量在a→b,发生的反应为:I2+HSO3-+H2O=I-+SO42-+3H+。
A.A点时,10mL0.2mol·L-1的KIO3溶液中的KIO3恰好完全被亚硫酸氢钠还原为I2,由原子守恒可知,n(I2)=![]() n(KIO3)=
n(KIO3)=![]() ×0.2×10×10-3=1.0×10-3mol,选项A正确;
×0.2×10×10-3=1.0×10-3mol,选项A正确;
B.2IO3-+5HSO3-=5SO42-+I2+H2O+3H+,由离子方程式可知,0a消耗的亚硫酸氢钠的物质的量为:2.5×0.2×10×10-3=5.0×10-3mol;加入NaHSO3的物质的量在a→b,发生的反应为:I2+HSO3-+H2O=I-+SO42-+3H+,故ab消耗的亚硫酸氢钠的物质的量恰好与1.0×10-3molI2完全反应,所以ab消耗的亚硫酸氢钠的物质的量1.0×10-3mol,0a:ab=(5.0×10-3mol):(1.0×10-3mol)=5:1,选项B错误;
C.当溶液中的n(I2)=5×10-4mol时,n(I2)=5×10-4mol<1.0×10-3mol,故有两种情况,一种情况是在0→a,向10mL0.2mol·L-1的KIO3溶液中逐渐加入NaHSO3粉末,刚好生成n(I2)=5×10-4mol,由2IO3-+5HSO3-=5SO42-+I2+H2O+3H+反应方程式可知,此时消耗亚硫酸氢钠的物质的量为:5×5×10-4mol=2.5×10-3mol;另一种情况是当10mL0.2mol·L-1的KIO3溶液中的KIO3恰好完全被亚硫酸氢钠还原为I2,有一部分的I2被亚硫酸氢钠还原为I-,消耗的亚硫酸氢钠的物质的量为5.0×10-3mol+5×10-4mol=5.5×10-3mol,选项C正确;
D.ab段发生的反应为I2+HSO3-+H2O=I-+SO42-+3H+,氧化性I2>HSO3-,选项D正确;
答案选B。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别为A、B、C、D四种短周期元素的最高价氧化物对应的水化物,已知0.1mol·L-1甲、丙、丁溶液的pH与A、C、D的原子序数关系如图所示(lg2=0.3),且常温下甲、丙、丁均可与乙反应。下列说法正确的是( )
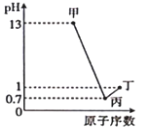
A.简单离子半径: D>C>B>A
B.A、C形成的化合物水溶液呈碱性
C.C、D形成的氢化物稳定性:C>D
D.A、B分别与D形成的化合物均为离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸是生活中常见的有机物之一,不仅是食醋的主要成分,在工业上也可用于制氢,已知如下反应:
热裂解反应:![]()
![]()
脱羧基反应:![]()
![]()
合成乙酸反应:![]()
![]()
(1)请写出![]() 与
与![]() 甲醇化的热化学方程式________。
甲醇化的热化学方程式________。
(2)在密闭容器中,利用乙酸制甲烷,若要使甲烷的产率较高,制备时选择的适宜条件为________。
a.较低温度 b.较大压强 c.高温 d.低压
(3)向一恒容密闭容器充入一定量的乙酸气体发生反应,相同时间后,测得温度与气体产率的关系如图:
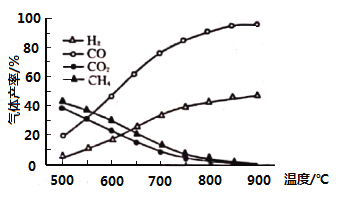
①约![]() 之前氢气产率低于甲烷的可能原因是________。而
之前氢气产率低于甲烷的可能原因是________。而![]() 之后氢气产率高于甲烷的理由是________。
之后氢气产率高于甲烷的理由是________。
②一定温度下,若在充入容器的乙酸气体中掺杂一定量水蒸气,氢气产率显著提高而![]() 产率下降,原因是________(用化学方程式表示)。
产率下降,原因是________(用化学方程式表示)。
(4)温度为![]() 时,在密闭容器中充入一定量乙酸气体,若利用合适的催化剂控制不发生其他的副反应,达到平衡时总压强为
时,在密闭容器中充入一定量乙酸气体,若利用合适的催化剂控制不发生其他的副反应,达到平衡时总压强为![]() ,热裂解反应消耗乙酸
,热裂解反应消耗乙酸![]() ,脱羧基反应消耗乙酸
,脱羧基反应消耗乙酸![]() ,乙酸的体积分数为________;脱羧基反应的平衡常数
,乙酸的体积分数为________;脱羧基反应的平衡常数![]() =________
=________![]() (
(![]() 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 Kx[Cu(C2O4)y]·zH2O (水合草酸铜(Ⅱ)酸钾)是一种化工原料,实验室制备少量水合草酸铜酸钾并测定样品的组成,实验步骤如下:
I制备CuO
用图1所示装置将溶液混合后,小火加热至蓝色沉淀变黑色生成CuO,煮沸5~10分钟。稍冷却后全部转移至图2装置过滤,并用蒸馏水洗涤沉淀2~3次。
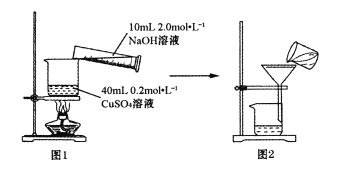
(1)①指出图2装置中操作中的错误___________,图2操作需用蒸馏水洗涤沉淀2~3次,其目为___________。
②检验沉淀洗涤干净的方法为___________。
Ⅱ制备KHC2O4和K2C2O4混合溶液
称取3.0g H2C2O4·2H2O放入250mL烧杯中,加入40mL蒸馏水,微热(温度低于80℃)溶解。稍冷后分数次加入2.2g无水K2CO3,充分反应后生成含KHC2O4和K2C2O4的混合物。
(2)该步骤中所得混合物中n(KHC2O4):n(K2C2O4)=____________。(取整数)
Ⅲ制备水合草酸铜酸钾晶体
将KHC2O4和K2C2O4混合溶液水浴微热,再将CuO连同滤纸一起加入到该溶液中,充分反应至CuO沉淀全部溶解,取出滤纸后,加热浓缩、冷却结晶、过滤,用乙醇淋洗,自然晾干,称量得到样品2.9760g(电子天平称量)。
(3)①步骤Ⅲ中KHC2O4的作用是__________。
②用乙醇淋洗而不用水的优点是__________。
③溶解CuO沉淀时,连同滤纸一起加人到溶液中的目的是__________。
Ⅳ测定水合草酸铜酸钾晶体的成分
取少量制得的样品配成溶液。用标准酸性髙锰酸钾溶液滴定![]() 、用标准EDTA溶液(PAR为指示剂)滴定Cu2+,经计算样品中n(Cu):n(
、用标准EDTA溶液(PAR为指示剂)滴定Cu2+,经计算样品中n(Cu):n(![]() )=1:2,假设制备样品的过程中Cu2+无损耗。
)=1:2,假设制备样品的过程中Cu2+无损耗。
(4)水合草酸铜(Ⅱ)酸钾晶体的化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如下:
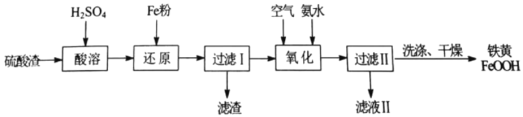
(1)“酸溶”时加快溶解的方法可以是________。(写出一种)
(2)“还原”过程中主要反应的离子方程式为________。
(3)“氧化”过程中,生成FeOOH的离子方程式为________。
(4)“过滤Ⅱ”所得铁黄在洗涤过程中,检验铁黄表面已洗涤干净的操作是________。
(5)实验测得反应溶液的![]() 、温度对铁黄产率的影响如图1、图2所示。
、温度对铁黄产率的影响如图1、图2所示。
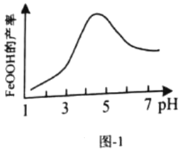
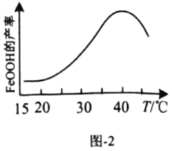
①反应温度宜选择________;
②氧化时应控制pH的合理范围是4.5左右,pH过小或过大均会导致铁黄产率较低,其可能原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.1L0.1mol·L-1CH3COOH溶液中逐渐加入NaOH固体,恢复至原温度后溶液中离子浓度关系如下图所示(忽略溶液体积变化)。下列有关叙述正确的是

A.25℃,CH3COOH的Ka数量级为10-4
B.B点:加入的NaOH的物质的量为0.005mol
C.A点:c(CH3COO-)+c(OH-)+c(CH3COOH)-c(H+)>0.1mol·L-1
D.A到C的过程中不考虑温度变化: 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A.金属发生电化学腐蚀的正极反应式:M-ne-=Mn+
B.家用小苏打溶于水后的电离:NaHCO3=Na++H++CO![]()
C.氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+H+
D.用碳酸钠溶液处理锅炉水垢中的硫酸钙:CaSO4(s)+CO![]() (aq)CaCO3(s)+SO
(aq)CaCO3(s)+SO![]() (aq)
(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“对氨基苯甲酸丁酯”是防晒霜中能吸收紫外线的防晒剂。下列关于“对氨基苯甲酸丁酯”的说法中正确的是( )
A.它的分子式为C11H15NO2
B.它能与盐酸反应,但不能与苛性钠溶液反应
C.甲酸丁酯基(—COOC4H9)有3种同分异构体
D.从有机物分类看,它可属于氨基酸类、酯类、芳香类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】初始温度为t ℃,向三个密闭的容器中按不同方式投入反应物,发生如下反应:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
容器 | 容器类型 | 初始体积 | 初始压强/Pa | 反应物投入量/mol | 平衡时Cl2的物质的量/mol | |||
HCl | O2 | Cl2 | H2O | |||||
I | 恒温恒容 | 1L |
| 4 | 1 | 0 | 0 | 1 |
II | 绝热恒容 | 1L | p2 | 0 | 0 | 2 | 2 | a |
III | 恒温恒压 | 2L | p3 | 8 | 2 | 0 | 0 | b |
下列说法正确的是( )
A.反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
B.a>1, b>2
C.p2=1.6×105Pa,p3=4×105Pa
D.若起始向容器Ⅰ中充入0.5 mol HCl、0.5 mol O2、0.5 mol Cl2和0.5 mol H2O,则反应向逆反应方向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com