
下列物质中,属于电解质且能导电的是
( )
A.铜片 B.硫酸溶液 C.熔融的氯化钠 D.固体氯化钾
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
下列关于F、Cl、Br、I性质的比较,不正确的是( )
|
| A. | 它们的原子核外电子层数随核电核数的增加而增多 |
|
| B. | 被其它卤素单质从其卤化物中置换出来的可能性随核电核数的增加而增大 |
|
| C. | 它们的氢化物的稳定性随核电核数的增加而增强 |
|
| D. | 单质的颜色随核电核数的增加而加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
判断下列有关化学基本概念的依据正确的是 ( )
A.溶液与胶体:不 同的本质原因是能否发生丁达尔效应
同的本质原因是能否发生丁达尔效应
B.纯净物与混合物:是否仅含有一种元素
C.氧化还原反 应:元素化合价是否变化
应:元素化合价是否变化
D.电解质与非电解质:物质本身的导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
溴被称为“海洋元素”,海水中的溴主要以NaBr
的形式存在。查阅资料得知:Br2的沸点为59℃,微溶于水,易溶于有机溶剂。实验室简单模拟从海水(此
处以低浓度的NaBr溶液代替)中提取溴单质的流程如图:


(1)写出实验操作的名称,操作① 、操作② ;
(2)在富集过程中,有如 下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
A.2NaBr+Cl2 = 2NaCl+Br2
B.2H2S+SO2 = 2H2O+3S↓
C.AlCl3+3NaAlO2+6H2O = 4Al(OH)3↓+3NaCl
D.Cl2 + 2NaOH = NaCl +NaClO + H2O
(3)实验前检测分液漏斗没有问题,但在操作 ①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因是 ;
①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因是 ;
(4)下列说法正确的是 。
A.操作①中,可以用酒精代替CCl4
B.操作②中,若发现忘了加碎瓷片,应该趁热补加
C.操作②中,温度计水银球应浸没在蒸馏烧瓶中液体的液面以下,但不能接触瓶底
D.操作②中,冷凝水流向应该是下进上出
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的a L HCl(g)溶于1000g水中,得
到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是( )
A.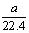 mo1·L-1 B.
mo1·L-1 B. mol·L-1 C.
mol·L-1 C. mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液可能含有Cl-、SO 、CO
、CO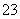 、NH
、NH 、Fe3+、Fe2+、
、Fe3+、Fe2+、
Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
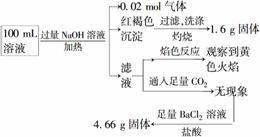
下列说法正确的是( )
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.要确定原溶液中是否含有Fe2+,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量
氯水,溶液呈血红色,则含有Fe2+
C.SO 、NH
、NH 、Na+一定存在,CO
、Na+一定存在,CO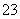 ,Al3+一定不存在
,Al3+一定不存在
D.溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是中学化学中常见物质的转化关系,部分物质和反应条
件略去。
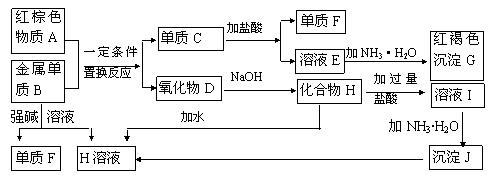

(1)单质F的化学式是________ ,写出物质A的一种用途 。
(2)写出单质B与强碱溶液反应的离子方程式 ,
写出由沉淀J生成 H溶液的离子方程式 ,
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:
,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式  。
。
(4)溶液I中所含金属离子是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,将等物质的量的P与Q投入体积固定2L密闭容器中,发生反应2P(g)+Qg)⇌xW(g)+U(g),经5min后到达平衡,这5min内W的平均反应速率是0.2mol/(L•min),平衡时U的浓度为0.5mol/L,[P]:[Q]=1:2,下列说法中不正确的是( )
|
| A. | x值是2 |
|
| B. | P平衡转化率为66.7% |
|
| C. | 平衡常数为1 |
|
| D. | 反应前,Q的物质的量为3 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com