
����Ŀ����ͬ�¶ȡ���ͬ�ݻ����ĸ��ܱ������н���ͬ���Ŀ��淴Ӧ��2X(g)+Y(g)![]() 3W(g)+2Z(g) ��H=��Q KJ/mol����ʼʱ������������ʵ�����ƽ��ʱ��ϵ�����仯�������������˵����ȷ���ǣ�������
3W(g)+2Z(g) ��H=��Q KJ/mol����ʼʱ������������ʵ�����ƽ��ʱ��ϵ�����仯�������������˵����ȷ���ǣ�������
X | Y | W | Z | ��Ӧ��ϵ�����仯 | |
�� | 2mol | 1mol | �ų�a kJ/mol | ||
�� | 1mol | 1mol | �ų�b kJ/mol | ||
�� | 2mol | 2mol | �ų�c kJ/mol | ||
�� | 3mol | 2mol | ����d kJ/mol |
A.X��ת����Ϊ���ף��ң���
B.c+d��Q
C.ƽ��ʱ���������еķ�Ӧ���ʱȶ������е���
D.ƽ��ʱ��������Z�����ʵ���Ũ�����
���𰸡�D
��������
A���������ʵ������ҵ�2�������ʵ�������ѹǿ����ת���ʼ�С����ת������>����������ȣ�����������X�����ʵ�������X��ת���ʼ�С����ת���ʼף��ң��������ʵ����൱���ڼĻ�����������Y����X��ת�������ף���������X��ת����Ϊ����>��>�ף���A����
B�������ڵ�Чƽ�⣬���߷�Ӧ�����෴�����ߵ�ת����֮��Ϊ100%���������֮��ΪQ�����ļ���Y�������ڼף�����������еij̶ȴ����Ա��ų����������ڼף����������֮�ʹ���Q����c+d>Q����B����
C�����ݷ�Ӧ2X(g)+Y(g)![]() 3W(g)+2Z(g)��֪���ں��º��������£���ʼʱ2molX��1molY�൱�ڼ���3molW��2molZ����������ƽ�⻥Ϊ��Чƽ�⣬��ƽ��ʱ�����Ũ����ȣ�����ƽ��ʱ�ס��������еķ�Ӧ������ȣ���C����
3W(g)+2Z(g)��֪���ں��º��������£���ʼʱ2molX��1molY�൱�ڼ���3molW��2molZ����������ƽ�⻥Ϊ��Чƽ�⣬��ƽ��ʱ�����Ũ����ȣ�����ƽ��ʱ�ס��������еķ�Ӧ������ȣ���C����
D�����п��Կ����ȼ���2molX��1molY��ƽ����ּ���1molY������Ӧ���Ũ��ƽ�������ƶ��������������Ũ����������Z�����ʵ���Ũ�����D��ȷ��
�ʴ�Ϊ��D��


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£������ܱ������ڷ�����Ӧ��H2(g)+I2 (g) ![]() HI(g) �� H< 0�����¶��£� K=43��ijʱ�̣���������� H2��I2��HI ��Ũ������Ϊ 0.01 mol/L��0.01mol/L��0.02mol/L�� һ��ʱ��������������ʵ�������
HI(g) �� H< 0�����¶��£� K=43��ijʱ�̣���������� H2��I2��HI ��Ũ������Ϊ 0.01 mol/L��0.01mol/L��0.02mol/L�� һ��ʱ��������������ʵ�������
A.���������������СB.��������ܶȱ��
C.���������ɫ����D.������ѹǿ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ž��з���Ԫ��������150���ꡣ�±���Ԫ�����ڱ���һ���֣�W��X��Y��ZΪ����������Ԫ�أ�W��X������ϼ�֮��Ϊ8������˵���������

A. ԭ�Ӱ뾶��W<X
B. ���³�ѹ�£�Y����Ϊ��̬
C. ��̬�⻯�����ȶ��ԣ�Z<W
D. X������������ˮ������ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼʵ��װ�ý������ʵ�飬�ܵó���Ӧʵ����۵��ǣ� ��
a | b | c | ʵ����� |
| |
A | Ũ���� | CaCO3 | C6H5ONa��Һ | ���ԣ�̼����� | |
B | Br2�ı���Һ | ��м | AgNO3��Һ | ����Һ�巢��ȡ����Ӧ | |
C | Ũ���� | ����KMnO4��Һ | �⻯����Һ | �����ԣ�Cl2��I2 | |
D | ����ʳ��ˮ | ��ʯ | ����KMnO4��Һ | ��Ȳ���л�ԭ�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӣ�Ni-Cd���ɳ�������ִ��������й㷺Ӧ�á��������ҺΪKOH��Һ����ط�ӦΪ��Cd +2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2�������й����ӵ�ص�˵����ȷ����
Cd(OH)2+2Ni(OH)2�������й����ӵ�ص�˵����ȷ����
A. �������ǻ�ѧ��ת��Ϊ���ܵĹ���
B. ���ʱ������ӦΪCd(OH)2��2e��="=" Cd + 2OH-
C. �ŵ�ʱ����ڲ�OH - �������ƶ�
D. ���ʱ��ֱ����Դ���������ĵ缫�Ϸ���Ni(OH)2ת��ΪNiO(OH)�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����
��3lg�������1.5NA��P-P��
��1L0.1mol��L-1��Na2CO3��Һ�����������ӵ�����ĿΪ0.1NA
�۱�״���£�22.4LHF �к���NA������
�ܵ�⾫��ͭʱ����ת��NA�����ӣ��������ܽ�32gͭ
�ݽ�2.24L(��״��)Cl2����ˮ��ת�Ƶĵ�����Ϊ0.1NA
�����£�����0.2molH2SO4��Ũ����������ͭ��Ӧ������SO2���ӵ���ĿС��0.1NA
��142gNa2SO4 ��Na2HPO4�Ĺ����������������������ӵ�����ĿΪ3NA
��NA��Fe(OH)3�������ӵ�����Ϊ107g
A.2��B.3��C.4��D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25����101 kPa�£�2g����ȼ������Һ̬ˮ���ų�285.8kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A. 2H2(g)+O2(g) == 2H2O(1) ��H�� �D285.8kJ��mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) ��H�� +571.6 kJ��mol
C. 2H2(g)+O2(g) == 2H2O(g) ��H�� �D571.6 kJ��mol
D. H2(g)+1/2O2(g) == H2O(1) ��H�� �D285.8kJ��mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ���Ը÷�Ӧ���ƶϺ������ǣ� ��

A.�÷�Ӧ�Ļ�ѧ����ʽΪ3B+2D![]() 6A+4C
6A+4C
B.��Ӧ���е�1sʱ��v��A��=3v��D��
C.��Ӧ���е�6sʱ�������ʵķ�Ӧ�������
D.��Ӧ���е�6sʱ��B��ƽ����Ӧ����Ϊ0.05mol/��Ls��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
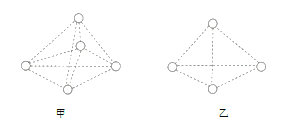
����Ŀ����ͼ��ʾ�Ǽ���Ͱ���![]() ���ӵĿռ�ṹʾ��ͼ���������Ϊ�ǻ�ѧ���ĸ�Ϊʵ�ߣ���ͼ�ϸļ��ɣ�����̼ԭ��Ϳ��ʵ��СԲ��_____��������ӵĿռ�ṹ��__________��������������������ͼ����ͼ�пɿ�����ÿ�������������__________�Թ��õ��Ӷԣ������������γ�__________�����ۼ���
���ӵĿռ�ṹʾ��ͼ���������Ϊ�ǻ�ѧ���ĸ�Ϊʵ�ߣ���ͼ�ϸļ��ɣ�����̼ԭ��Ϳ��ʵ��СԲ��_____��������ӵĿռ�ṹ��__________��������������������ͼ����ͼ�пɿ�����ÿ�������������__________�Թ��õ��Ӷԣ������������γ�__________�����ۼ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com