
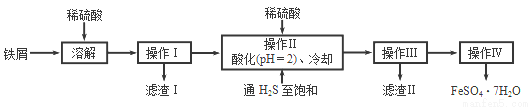
绿矾(FeSO4 • 7H2O)是治疗缺铁性贫血的特效药.下面是以商品级纯度铁屑(含少量锡等杂质)生产绿矾的一种方法:
已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH 为3.0,沉淀完全时的pH为5.5:
回答下列问题:
(1)操作Ⅱ中用硫酸酸化至pH=2且通入硫化氢至饱和的目的是:
①除去操作I所得溶液中含有的Sn2+等杂质离子;
②____________________________;
③____________________________。
(2)操作IV的顺序依次为:_______________、_______________、过滤、洗涤。
(3)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;②___________________。
(4)测定绿矾产品中Fe2+ 含量的方法是:a.称取8.680g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.02000 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为30.00 mL(滴定时发生反应的离子方程式为:5Fe2+ + MnO4- + 8H+ ═ 5Fe3+ + Mn2+ + 4H2O)
①计算上述样品中FeSO4 • 7H2O的质量分数为_________________(结果保留4位有效数字,FeSO4 • 7H2O的摩尔质量为 278g/mol)
②若用上述方法测定的样品中FeSO4•7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有:样品中存在少量的杂质、___________________
科目:高中化学 来源:2016-2017学年安徽省六安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列氯化物中既能由单质直接化合制得,又可由金属和盐酸反应制得的是( )
A. CuCl2 B. FeCl2 C. FeCl3 D. AlCl3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:填空题
如图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由____逐渐变为____色,试管内的液面会逐渐_____________;当反应停止后向试管中缓慢通入氧气,气体颜色又由______色逐渐变为______色,之后又变为______色,试管内的液面会____________。用化学方程式表示试管中发生的化学反应_____________,____________。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:选择题
4.6g金属钠在干燥空气中被氧化后,得到7.0g固体,由此可判断其产物是 ( )
A. 只有Na2O B. 只有Na2O2 C. Na2O2和Na2O D. 无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各组中的离子,因发生氧化还原反应而不能大量共存同一溶液中的是:( )
A. Fe2+、SO42-、Fe3+ 、Cl- B. S2-、Cu2+、Na+、Cl-
C. H+、SO42-、Cu2+、OH- D. Fe2+、H+、Mg2+、NO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省新余市高二下学期入学考试化学试卷(解析版) 题型:选择题
利用海水提取溴和镁的过程如下,下列说法不正确的是( )

A. 若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2
B. 工业上常利用电解熔融MgCl2冶炼金属镁
C. 富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D. 工业溴中含少量Cl2,可用NaOH溶液除去
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省新余市高二下学期入学考试化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族。下列说法正确的是( )
A. 元素Y、W的简单阴离子具有相同的电子层结构
B. 由X、W两种元素组成的化合物是离子化合物
C. X的简单气态氢化物的热稳定性比W的强是因为X的氢化物分子间易形成氢键
D. 离子半径:r(Z)<r(Y)<r(X)<r(W)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二2月月考化学试卷(解析版) 题型:选择题
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
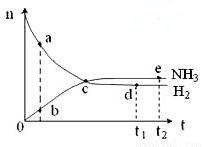
A. 点a的n(H2)和点b的n(NH3)比值为3∶2
B. 点 c处反应达到平衡
C. 点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D. 其他条件不变,773K下反应至t1时刻,n(H2)比右图中d点的值大
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:简答题
工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
已知:
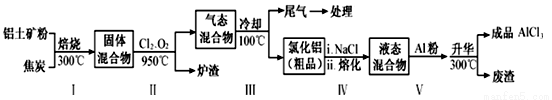
物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
(1)步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是_________________(只要求写出一种)。
(2)步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是________________。
(3)结合流程及相关数据分析,步骤V中加入铝粉的目的是________________。
(4)称取含Fe2O3和Al2O3的试样0.2000g,将其溶解在pH=2.0的热溶液中(50℃左右),以磺基水杨酸为指示剂,用0.02000 mol/L EDTA标准溶液滴定试样中的Fe3+,用去18.00 mL。然后将试液调至pH=3.5,加入上述EDTA标准溶液25.00 mL,并加热煮沸,使Al3+与EDTA完全反应,再调试液pH=4.5,以PAN(1-(2-吡啶偶氨)-2-萘酚)为指示剂,趁热用CuSO4标准溶液(每毫升含CuSO4·5H2O 0.005000g)返滴定,用去8.00 mL。计算试样中Fe2O3和Al2O3的质量分数。________________(写出计算过程)
(已知:EDTA与Fe3+、Al3+、Cu2+均按物质的量之比1∶1进行反应)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com