
| A.若把HF分子写成H2F分子,违反了共价键的饱和性 |
B.若把碳的轨道式写成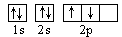 则违反了泡里不相容原理 则违反了泡里不相容原理 |
| C.若把Be的基态电子排布式写成1s22s12p1 则违反了能量最低原理 |
D.若把氧的轨道式写成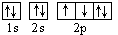 则违反了洪特规则 则违反了洪特规则 |
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.在含有多个电子的原子里,电子是分层排布的 |
| B.在原子核外的各电子层中,能量高的离核近,能量低的离核远 |
| C.在原子核外的各电子层中,层数大的能量高,层数小的能量低 |
| D.在原子核外的各电子层中,层数大的离核远,层数小的离核近 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物的熔点一定高于共价化合物 |
| B.由盐酸的酸性强于氢硫酸,可知氯元素的非金属性强于硫元素 |
| C.共价化合物中只存在共价键,离子化合物中一定含有离子键 |
| D.第二周期元素的最高正化合价从左到右依次升高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 102 | 74 |
| 主要化合价 | +2 | +3 | +6、+4、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱性:NaOH>Mg(OH)2 | B.热稳定性:NH3>PH3 |
| C.金属性:K>Na | D.原子半径:Cl>S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com