
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |

分析 根据元素在周期表中的相对位置可知,A为H元素、B为He、C为Na、D为C、E为N、F为O、G为Si、H为Cl元素,
(1)有机物中都含有C原子,所以碳元素形成的化合物种类最多;
(2)非金属性越强,对应气态氢化物的稳定性越强,根据二者的非金属性判断;
(3)A为H、E为N,二者形成的极易溶于水的化合物为氨气,氨气为共价化合物,分子中存在3个氮氢键,据此写出其电子式;
(4)氯气与水反应生成氯化氢和次氯酸,所以氯水显示酸性,同时生成的次氯酸具有漂白性;
(5)过氧化钠和二氧化碳反应生成氧气,过氧化钠可以做呼吸的供氧剂.
解答 解:根据元素在周期表中的相对位置可知,A为H元素、B为He、C为Na、D为C、E为N、F为O、G为Si、H为Cl元素,
(1)上述元素A、B、D、E、F中形成化合物种类最多的一种元素为C元素,C的原子序数为6,其原子结构示意图为: ,
,
故答案为: ;
;
(2)D的氢化物为甲烷,G的氢化物硅烷,非金属性:C>Si,非金属性越强,对应的气态氢化物越稳定,则气态氢化物D的氢化物>G的氢化物,
故答案为:>;
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物为氨气,氨气为共价化合物,氨气电子式为: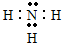 ,
,
故答案为;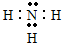 ;
;
(4)现有上表中所列字母代表的某一种元素,其单质通入到紫色石蕊溶液中的现象为先变红后褪色,该单质为氯气,氯气与水反应生成氯化氢和次氯酸,反应的离子方程式为:Cl+H2O=H++Cl-+HClO,
故答案为:Cl+H2O=H++Cl-+HClO;
(5)过氧化钠和二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;为稀释氧气,制造一种适合宇航员生存的人工生态环境,可以在飞船中加氮气,制造类似空气的环境,氮气的结构式为:N≡N,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;N≡N.
点评 本题考查元素周期表与元素周期律的综合应用,题目难度中等,熟悉元素在周期表中的位置并推出元素是解答本题的关键,并熟悉元素及其单质、化合物的性质即可解答.


科目:高中化学 来源: 题型:解答题

| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化氮中混有一氧化氮杂质,可通入氧气将一氧化氮转化为二氧化氮 | |
| B. | 过量的铜与浓硝酸反应一定有一氧化氮生成 | |
| C. | Fe与S混合加热生成FeS2 | |
| D. | 工业上利用氨气制硝酸属于人工固氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是氧化物 | |
| B. | 含有K、Cr、O三种元素 | |
| C. | 钾、铬、氧三种元素的质量比为 39:52:112 | |
| D. | 重铬酸钾是由2个钾原子、2个铬原子、7个氧原子构成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 2min | 4min | 6min | 8min | ′′′ | |
| CO | 0.07 | 0.06 | 0.04 | 0.05 | ′′′ |
| H2 | x | 0.12 | 0.12 | 0.2 | ′′′ |
| CH2OH | 0.03 | 0.04 | 0.04 | 0.05 | ′′′ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com