
【题目】下列各组化合物中,所含元素种类相同的是
A. 纤维素和抗体 B. DNA和磷脂 C. 叶绿素和核糖核酸 D. 血红蛋白和脂肪
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】硫在自然界中以游离态和多种化合态形式出现。硫的化合物大多具有氧化性或还原性。
(1)硫化氢具有还原性,可以和许多氧化剂反应。H2S的水溶液称作氢硫酸, 氢硫酸在空气中放置,很快出现浅黄色硫单质,写出反应的化学方程式____________________。该实验用于比较物质氧化性和还原性的强弱,可得出如下结论:氧化性:______________;还原性:__________________。
(2)在酸性条件下,KMnO4和少量H2S反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式。并用单线桥标出电子转移的方向和数目:____________________。
(3)将黑色的Fe2S3固体加入足量盐酸中,溶液中有淡黄色硫生成,产物还有____、______。过滤,微热滤液,然后加入过量的氢氧化钠溶液,可观察到的现象是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为建设“蓝天常在、青山常在、绿水常在”的美丽中国,2015年4月16日国务院颁布了《水污染防治行动计划》。下列做法不利于该目标实现的是
A. 推广使用无磷洗涤剂B. 用O3替代Cl2作饮用水消毒剂
C. 用工业污水直接灌溉农田D. 含Cr3+的废水用适量石灰处理后排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,下列各组热化学方程式中Q2>Ql的是
A. 2H2(g)+O2(g)=2H2O(g);△H=-Q1 2H2(g)+O2(g)=2H2O(1); △H=-Q2
B. S(g)+O2(g)=SO2(g); △H=-Q1 S(s)+O2(g)=SO2(g); △H=-Q2
C. C(s)+O2(g)=CO2(g); △H=-Q1 C(s)+1/2O2 (g)=CO(g); △H=-Q2
D. H2(g)+Cl2(g)=2HCl(g);△H=-Q1 1/2H2(g)+1/2Cl2(g)=HCl(g);△H=-Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置制备并检验Cl2的性质。

下列说法正确的是
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗
B. Ⅱ图中:量筒中发生了加成反应
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答:
(1)NO的体积,NO2的体积?
(2)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,求原硝酸溶液的浓度?
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 , 至少需要30%的双氧水多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.7.2g CaO2晶体中阴离子和阳离子总数为0.3NA
B.反应3H2(g)+N2(g)2NH3(g)△H=﹣92 kJ/mol放出热量9.2kJ时,转移电子0.6NA
C.0.1 mol/L NH4Cl溶液中Cl﹣离子数目为0.1NA
D.0.1 mol H2O2分子中含极性共价键数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、CO2的吸收利用对促进低碳社会的构建和环境保护具有重要意义。
(1)已知:① 2H2(g) + O2(g)=2H2O(g) H1
② CO2(g)+3H2(g)![]() CH3OH (l) + H2O (l) H2
CH3OH (l) + H2O (l) H2
③ H2O(g)![]() H2O(l) H3
H2O(l) H3
求 25℃、101kPa下,2 mol CH3OH (l)完全燃烧的H=_____(用含H1、H2、H3的式子表示)。
(2)向1 L密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) ![]() CH3OH (l) + H2O (l) H2
CH3OH (l) + H2O (l) H2
①已知反应的H2<0,则此反应自发进行的条件是_________(填“低温”、“高温”或“任意温度”)。
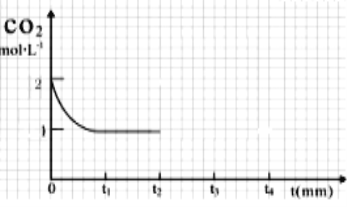
②在t2时将容器容积缩小为原体积的一半,t3时再次达到平衡,请画出t2之后 CO2气体的浓度随时间变化的曲线。______________
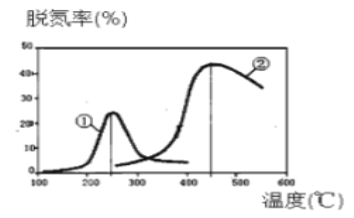
(3)用NH3催化还原NOX可以消除氮氧化物的污染。如下图,采用NH3作还原剂,烟气以一
定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为:NO(g) + NO2(g) + 2NH3(g)![]() 2N2(g) + 3H2O(g)。 以下说法不正确的是__________。(填编号)
2N2(g) + 3H2O(g)。 以下说法不正确的是__________。(填编号)
A.使用第②种催化剂更有利于提高NOx的平衡转化率
B.催化剂①、②分别适合于250℃和450℃左右脱氮
C.相同条件下,改变压强对脱氮率会有影响
D.烟气通过催化剂的流速越快,脱氮效果会越好
(4)用电解法处理NO2是消除氮氧化物污染的新方法,其原理是将NO2在电解池中分解成无污染的N2和O2,电解质是固体氧化物陶瓷(内含O2ˉ离子,可定向移动),阳极的反应式是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com