
在25 ℃时,将a g NH3完全溶于水,得到V mL pH=8的氨水,假设该氨水的密度为ρ g·cm-3,溶质的质量分数为ω,其中含NH4+的物质的量为b mol,下列叙述中错误的是( )
A.溶质的质量分数为ω= ×100%
×100%
B.溶质的物质的量浓度c= mol·L-1
mol·L-1
C.溶液中c(OH-)= mol·L-1
mol·L-1
D.上述溶液中再加入VmL水后,所得溶液的质量分数小于0.5ω
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
有关下列离子方程式的说法正确的是( )
A.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O
NH3↑+H2O
B.向NaAlO2溶液中 通入少量的CO2的反应为:2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—
通入少量的CO2的反应为:2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—
C.FeBr2与足量的Cl2反应为:2Fe2++2Br—+2Cl2=2Fe3++Br2+4Cl—
D.用浓 盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4—+6H++5H2O2=2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:实验题
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_____________。
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL 煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________。
(4)丙组同学取10 ml 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl3溶液混合。分别取 2 mL 此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有______(填离子符号),由此可以证明该氧化还原反应为____________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是________________,生成沉淀的原因是________________(用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源:2017届山西省大同市高三上学期第一次调研化学试卷(解析版) 题型:选择题
设NA为阿佛加德罗常数的值,下列叙述不正确的是( )
A.标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA
B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.标准状况下,22.4L氯气与足量铁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月质检化学试卷(解析版) 题型:选择题
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )

A.②代表滴加H2SO4溶液的变化曲线
B.b点溶液中大量存在的离子是SO42-、Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点两溶液中含有相同量的OH-
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月质检化学试卷(解析版) 题型:选择题
下列现象或事实不能用同一原理解释的是( )
A.浓硝酸和硝酸银用棕色试剂瓶保存
B.常温下铁和铂都不溶于浓硝酸
C.亚硫酸盐和硫酸亚铁固体长期暴露在空气中变质
D.H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率
查看答案和解析>>
科目:高中化学 来源:2017届山东省栖霞市高三上学期期中化学试卷(解析版) 题型:实验题
无水氯化铝是一种重要的化工原料,工业上利用明矾石制备无水氯化铝的流程如下,请回答下列问题:

(1) 实验室中,可制得Cl2的组合是____________(填代号)。
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热
③NaClO和盐酸混合共热 ④漂白粉和硫酸混合共热
(2) 吸收焙烧炉中产生的尾气,下列装置合理的是___________(填代号)。

(3)写出氧化炉中反应的化学方程式_____________。
(4)生产氯化铝的过程中焙烧炉和氯化炉中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少污染。试设计简单实验检验二者是否恰好完全反应,简要描述实验步骤、现象和结论_____________(仪器自选)。
可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氣化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某同学设计用如下装置验证二氧化硫的某些化学性质。
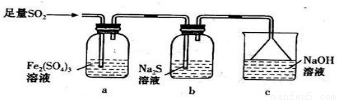
① 能说明二氧化硫具有氧化性的实验现象为____________。
② 写出a瓶中发生反应的离子方程式________________。
③ 充分反应后,取a瓶中的溶液分成三份,分别进行如下实验。
实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色。
实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去。
实验III:向第三份溶液中加人BaCl2溶液,生成白色沉淀。
上述实验中能充分证明二氧化硫具有还原性的是__________(填实验代号)。
查看答案和解析>>
科目:高中化学 来源:2017届山东省栖霞市高三上学期期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.Na2O与Na2O2都是碱性氧化物
B.生石灰能与水反应,可用来干燥氨气
C.从海水中提取物质都必须通过化学反应才能实观
D.氯化铝是一种离子型电解质.可用于电解法制铝
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月月考化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
选项 | 现象或事实 | 解释 |
A | Al(OH)3用作塑料的阻燃剂 | Al(OH)3受热熔化放出大量的热 |
B | 用氢氟酸蚀刻玻璃 | Si02是碱性氧化物,能溶于酸 |
C | 过氧化钠作呼吸面具中的供氧剂 | 过氧化钠是强氧化剂,能氧化二氧化碳 |
D | 用浸有酸性高锰酸钾溶液的硅藻土作水果保鲜剂 | 酸性高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com