
����Ŀ����������п��һ�ֶ���Ե����������ϣ�ijС���Դ�����п��������ͭ�������Ϊԭ��ģ�ҵ������������п���������£�

��֪����������������pH��Χ���±���ʾ��
Zn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
��ʼ����pH | 5.4 | 7.0 | 2.3 | 4.7 |
��ȫ����pH | 8.0 | 9.0 | 4.1 | 6.7 |
���������գ�
��1��Ϊ�˼ӿ��ȡ�ķ�Ӧ���ʣ����Բ�ȡ�Ĵ�ʩ_________________________________
��2������II�м���H2O2��Һ��������_________________________�������ӷ���ʽ��ʾ����
��3����ZnO����pH���Գ�ȥ�������ʣ�����pH�����˷�Χ��_______________________��
��4������III�м���Zn�۵������ǣ���__________________������һ��������ҺpH��
��5����ʽ̼��п[Zn2(OH)2 CO3]���յĻ�ѧ����ʽΪ________________________________��
��6�������·����ⶨ���û�������п�Ĵ��ȣ��������ʲ����뷴Ӧ����
�� ȡ1.000g��������п����15.00mL 1.000mol��L-1 ������Һ��ȫ�ܽ⣬���뼸�μ��ȡ��� ��Ũ��Ϊ0.5000mol��L-1 �ı�����������Һ�ζ�ʣ�����ᣬ�����յ�ʱ��������������Һ12.00mL���жϵζ��յ�ķ�����___________________________________________�����û�������п�Ĵ���Ϊ________________________
���𰸡����Ȼ��ʵ����������Ũ�Ȼ������2Fe2++H2O2+2H+=2Fe3++2H2O4.1��4.7��ȥ��Һ�е�Cu2+Zn2(OH)2CO3![]() 2ZnO+CO2��+H2O����Һ�ɳ�ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ��Ϊ�ζ��յ�97.2%
2ZnO+CO2��+H2O����Һ�ɳ�ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ��Ϊ�ζ��յ�97.2%
��������
������п��������ͭ�����������ϡ�����ܽ⣬���ˣ��õ���Һ�к�����������������ͭ������п������H2O2��Һ������������Ϊ�����ӣ��ټ�������п������ҺpHʹ��Һ��������ת���������˳�ȥ��������Һ����п���Խ�һ��������ҺpH������ԭͭ����Ϊͭ���ʣ����˳�ȥ���õ�����п��Һ������̼�����̼�����ɼ�ʽ̼��п�����ȷֽ����ɻ�������п���Դ˽�������
��1��������Һ�巴Ӧʱ�������ı�������Լӿ췴Ӧ���ʣ������¶ȡ��ʵ���������Ũ��Ҳ�ܼӿ췴Ӧ���ʣ�
�ʴ�Ϊ�����Ȼ��ʵ����������Ũ�Ȼ��������
��2������H2O2��Һ������������Ϊ�����ӣ�ͬʱ����ˮ����Ӧ���ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��3����ZnO����pH��ʹFe3+ת��Ϊ����������������ȥ���������ӳ�����ȫ��ͭ���ӿ�ʼ����pH��֪��������ҺPHΪ4.1��4.7��
�ʴ�Ϊ��4.1��4.7��
��4������III�м���Zn�۽�һ��������ҺpH������ԭͭ����Ϊͭ���ʣ����˳�ȥ��
�ʴ�Ϊ����ȥ��Һ�е�Cu2+��
��5����ʽ̼��п�Ļ�ѧʽΪZn2(OH)2 CO3���ֽ���������п��������̼��ˮ�����ԭ���غ���ƽ��д�õ���Ӧ�Ļ�ѧ����ʽΪ��Zn2(OH)2CO3![]() 2ZnO+CO2��+H2O��
2ZnO+CO2��+H2O��
�ʴ�Ϊ��Zn2(OH)2CO3![]() 2ZnO+CO2��+H2O��
2ZnO+CO2��+H2O��
��6�����ݵζ�ԭ����֪���ζ��յ�ʱ��Һ��ɫ�ɳ�ɫ��Ϊ��ɫ���Ұ���Ӳ���ɫ��Ϊ�ζ��յ���
����H++OH-=H2O��֪�����ᷴӦ��ʣ�����������ʵ���Ϊ0.500mol/L��0.0120L=0.006mol������ZnO��Ӧ�����������ʵ���Ϊ=0.0150L��1.000mol/L��2-0.006mol=0.024mol��
��ZnO+2H+=Zn2++H2O��֪��ZnO������Ϊ0.024mol��![]() ��81g/mol=0.972g��
��81g/mol=0.972g��
����Ʒ����Ϊ![]() ��100%=97.2%��
��100%=97.2%��
�ʴ�Ϊ������Һ�ɳ�ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ��Ϊ�ζ��յ㣻97.2%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѪҺ��Ca2����Ũ��һ�����mg/cm3����ʾ����ȡһ�������Ѫ�����������IJ����[(NH4)2C2O4]��Һ�������������(CaC2O4)���������˲���Ƴ���ϴ�Ӻ�����ǿ��ɵò���(H2C2O4)������KMnO4��Һ�ζ����ɲⶨѪҺ��Ʒ��Ca2����Ũ�ȡ�ij�о���ѧϰС���������ʵ�鲽��ⶨѪҺ��Ʒ��Ca2����Ũ�ȡ�
������KMnO4����Һ����ͼ������50 mL KMnO4����Һ�Ĺ���ʾ��ͼ��
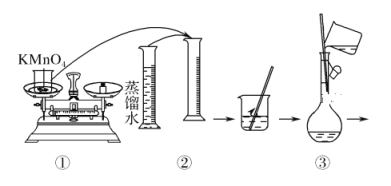
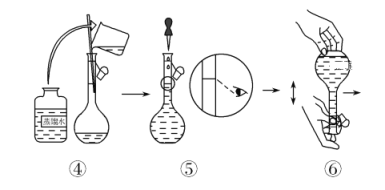
(1)����۲�ͼʾ�жϣ����в���ȷ�IJ�����(�����)________��
(2)����ȷ��50 mL��Һ�����������(������)________��
(3)�����ͼʾ�IJ���������Һ�������Ƶ���ҺŨ�Ƚ�________(�ƫ��ƫС��)��
���ⶨѪҺ��Ʒ��Ca2����Ũ�ȣ���ȡѪ��20.00 mL����������������õ����ᣬ����0.020 mol/L KMnO4��Һ�ζ���ʹ����ת����CO2�ݳ�����ʱ������12.00 mL KMnO4��Һ��
(4)��֪�����KMnO4��Һ��Ӧ�����ӷ���ʽΪ��
2MnO4-��5H2C2O4��6H��===2Mnx����10CO2����8H2O��ʽ�е�x��________��
(5)�������㣬ѪҺ��Ʒ��Ca2����Ũ��Ϊ________mg/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ X Y M N ��Ӧ�е������仯������ͼ���������ƶ�һ����ȷ���ǣ� ��

A. X ���������� M ������
B. Y ���������� N ������
C. X �� Y ���������� M �� N ������
D. �÷�Ӧ�����ȷ�Ӧ����Ӧ�����Ǽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ǻϳ������ص�ԭ�ϣ����������ȩ�ϳɣ�

�����й�������ȷ����
A. ���ȩ�ķ���ʽ��C8H10O3
B. ���ȩ����NaHCO3��Һ��Ӧ
C. �������ʾ�����������Ȼ�̼��Һ�����ӳɷ�Ӧ
D. ����FeCl3��Һ�������������Ƿ����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ͭ����ƽ�⣺Cu(OH)2 +2OH��![]() Cu(OH)42��������ɫ����ijͬѧ��������ʵ�飺
Cu(OH)42��������ɫ����ijͬѧ��������ʵ�飺
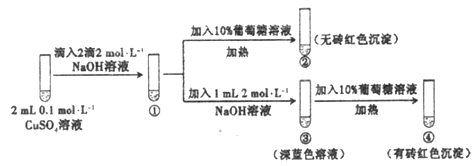
����˵������ȷ����
A. ���г�����ɫ����
B. ����������Cu(OH)2+ 2OH��![]() Cu(OH)42�������ƶ��Ľ��
Cu(OH)42�������ƶ��Ľ��
C. ��������֤�������Ǿ��л�ԭ��
D. �ԱȢںܿ͢�֪Cu(OH)2������ǿ��Cu(OH)42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ҵ��������屽����ķ����ǣ� ��
A. ���������B. �����Ը��������Һ��������
C. ������ˮ��������D. ����������Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ٹ��� ������ �۶����ЧӦ ������ �ݵ�Ӿ ��Һ�����û��������ᴿ���ǣ� ��
A.�٢ڢ�B.�٢ڢܢ�C.�٢ڢۢܢ�D.ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������з�Ӧ�У�����ֻ���������Ե��ǣ� ��
A. Cu+H2SO4��Ũ�� B. C+H2SO4��Ũ��
C. Ba(OH)2+H2SO4 D. FeO+H2SO4��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܽϺ�˵���Ҵ����ӽṹ��ʽΪC2H5OH��������CH3OCH3����ʵ�ǣ�������
A. 1mol�Ҵ���ȫȼ��ֻ����2molCO2��3molH2O
B. �Ҵ���ͬ���칹��
C. 0.1mol�Ҵ��������Ʒ�Ӧֻ����0.05mol����
D. �Ҵ���ˮ�������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com