
新型纳米材料氧缺位铁酸盐(MFe2Ox )(3<x<4,
M表示Mn、Co、Zn或Ni的二价离子),常温下,它能使工业废气中的SO2、NO2等氧化物转化为单质。
转化流程如图所示:
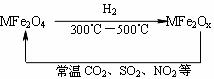
有关上述转化过程的下列叙述正确的是( )
A.  MFe2O4表现了还原性 B. MFe2Ox表现了还原性
MFe2O4表现了还原性 B. MFe2Ox表现了还原性
C. SO2和NO2表现了还原性 D. SO2和NO2发生了分解反应
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
进行化学实验必须注意安全,下列说法正确的是( )
A.不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
B.不慎将浓碱液沾到皮肤上,要立即用大量的稀硫酸冲洗
C.酒精灯着火时可用水扑灭
D.稀释浓硫酸时,可往装有一定体积浓硫酸的量筒中,慢慢加入水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验下列实验目的能实现的是 ( )
A.用10 mL 量筒量取5.2 mL盐酸 B.向小试管中加入100mL稀盐酸
C.用托盘天平称取25.12gNaCl固体 D.用100 mL容量瓶配制50mL0.1 mol/L的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式正确的是
A.NaHCO3= Na++ H++CO32- B.Ba(OH)2=Ba2++OH-
C.Al2(SO4)3=2Al3++3SO42- D.H2SO4=H2++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验室中常用加热分解氯酸钾制取氧气,写出反应的化学方程式,并用双线桥法标出电子转移情况: 。
(2)实验室制取Cl2的反应方程式之一为: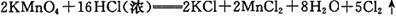 。
。
被氧化的盐酸占反应盐酸总量的 ;
当标准状况下有11.2L氯气生成时,该反应的电子转移数为 。
(3)已知下列两个氧化还原反应:O2+4HI===2I2+2H2O 及Na2S+I2===2NaI+S,则三种单质的氧化性顺序为:
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式: ;在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式: 。
(5)医疗上常用小苏打治疗胃酸过多,小苏打溶液与盐酸反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105 Pa, 32 g O2和O3的混合气体所含原子数为2NA
C.标准状况下,11.2LH2O 含有的分子数为0.5NA
D.在常温常压下,44gCO2含有的分子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列做法会对人体健康造成较大危害的是( )
A.用大量SO2漂白银耳
B.用小苏打(NaHCO3)焙制糕点
C.用食醋清洗热水瓶胆内壁附着 的水垢(CaCO3)
的水垢(CaCO3)
D.用消毒液(有效成分NaClO)对餐具进行杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质,用编号填空回答下列问题:
A.干冰 B.金刚石 C.氦 D.过氧化钠 E.二氧化硅 F.溴化铵
(1)通过非极性键形成的原子晶体是: .
(2)可由原子直接构成的晶体是: .
(3)含有离子键、共价键、配位键的化合物是: .
(4)含有非极性键的离子化合物是: .
(5)已知微粒间的作用力包括离子键、共价键、金属键、范德华力、氢键.氯化钠熔化,粒子间克服的作用力为 ;二氧化硅熔化,粒子间克服的作用力为 ;干冰气化,粒子间克服的作用力为 .A、B、C、D四种物质的熔点从低到高的顺序为 (填序号).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com