
����Ŀ��Ī��ɳ����Ҫ�������ƺ�������Ⱦ������LΪ�ϳ�Ī��ɳ�ǵ��м��壬��ϳ�·��������

��֪��ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ�![]()
(1)A�Ļ�ѧ����Ϊ______��B�еĹ�����������______��
(2)E�����й�ƽ��ԭ����Ŀ���Ϊ________��
(3)����G�ķ���ʽΪC6H7N������ӵĺ˴Ź�����������______�����շ塣
(4)̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼ԭ�ӳ�Ϊ����̼ԭ�ӡ�д��L�Ľṹ��ʽ�����Ǻ�(*)���L�е�����̼ԭ��______________________��
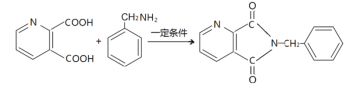
(5)��֪1 mol ����J ������NaHCO3��Һ��Ӧ����2 mol CO2��д��D��J��K�Ļ�ѧ����ʽ_________________________________________________��
(6)X�ǽ�H���ӽṹ�е�-CHO��Ϊ-NH2��ͬ���칹�壬��X���������ĸ�ȡ������ ����������������X��________�֡�
���𰸡��ױ� ��ԭ�� 7 4 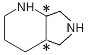
 +2H2O 11
+2H2O 11
��������
�ױ��ڹ��������£�����������ȡ������ȡ����Ӧ������C7H6Cl2�� ������������ˮ��Һ�����·���ˮ�ⷴӦ������ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ�
������������ˮ��Һ�����·���ˮ�ⷴӦ������ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ�![]() ���������ɱ���ȩ���ڰ����������������£���Ӧ����C7H9N���ṹ��ʽΪ
���������ɱ���ȩ���ڰ����������������£���Ӧ����C7H9N���ṹ��ʽΪ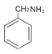 ������һ��·�ߣ���ϩ����������Ӧ�õ�CH2=CHCHO���������Ʒ���HΪ
������һ��·�ߣ���ϩ����������Ӧ�õ�CH2=CHCHO���������Ʒ���HΪ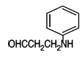 ����G��CH2=CHCHO�ӳɵõ�����GΪ
����G��CH2=CHCHO�ӳɵõ�����GΪ![]() ��I���������������õ�J���ݴ˻ش����⡣
��I���������������õ�J���ݴ˻ش����⡣
(1)A�Ļ�ѧ����Ϊ�ױ�������B�Ľṹ��֪����������������ԭ�ӡ�
(2)E���Ӿ��м���̼̼˫��Ϊƽ��ṹ����ƽ��ԭ����Ŀ���Ϊ7����
(3)����G�ķ���ʽΪ C6H7N���ṹΪ![]() ������ӵĺ˴Ź�����������4�����շ塣
������ӵĺ˴Ź�����������4�����շ塣
(4) L�Ľṹ��ʽΪ ��̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼ԭ�ӳ�Ϊ����̼ԭ�ӣ�*Ϊ����̼ԭ�ӣ����ʾΪ
��̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼ԭ�ӳ�Ϊ����̼ԭ�ӣ�*Ϊ����̼ԭ�ӣ����ʾΪ  ��
��
(5)��֪1 mol ����J ������NaHCO3 ��Һ��Ӧ����2 mol CO2��˵��J����2���Ȼ�������K�ṹ���ƿ�֪��JΪ ��D��J��K�Ļ�ѧ����ʽ
��D��J��K�Ļ�ѧ����ʽ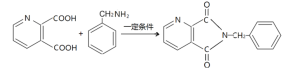 +2H2O��
+2H2O��
(6)HΪ ��X�ǽ�H���ӽṹ�е�-CHO��Ϊ-NH2��ͬ���칹�壬X���������ĸ�ȡ����������������������������������Ϲ��ɣ�����������X��11�֡�
��X�ǽ�H���ӽṹ�е�-CHO��Ϊ-NH2��ͬ���칹�壬X���������ĸ�ȡ����������������������������������Ϲ��ɣ�����������X��11�֡�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�ѧ�������������ת����˵����ȷ���ǣ� ��

A. ͼ1��ʾ��װ���ܽ���ѧ��ת��Ϊ����
B. ͼ2��ʾ�ķ�ӦΪ���ȷ�Ӧ
C. �кͷ�Ӧ�У���Ӧ��������������������������
D. ��ѧ��Ӧ�������仯����Ҫԭ���ǻ�ѧ���Ķ������γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���1molPCl5ͨ��һ���ݻ��̶�������ܱ������У�������Ӧ��PCl5(g) ![]() PCl3(g) + Cl2(g)����Ӧ�ﵽƽ��ʱ�����PCl5Ϊ0.4mol����ʱ����������ͨ��1mol PCl5��ͬ���¶����ٴﵽƽ��ʱ�����PCl5Ϊamol�������ж���ȷ���ǣ� ��
PCl3(g) + Cl2(g)����Ӧ�ﵽƽ��ʱ�����PCl5Ϊ0.4mol����ʱ����������ͨ��1mol PCl5��ͬ���¶����ٴﵽƽ��ʱ�����PCl5Ϊamol�������ж���ȷ���ǣ� ��
A.Cl2�������������B.PCl5��ת��������
C.a =0.8D.a > 0.8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������������Ա�ӳ���ȡ����������Ʒ1.00mL ����ƿ�У���25mL ˮϡ�ͣ����������ữ����μ���0.1000mol��L-1KMnO4 ��Һ������Ӧ��ȫʱ������KMnO4��Һ20.20mL���Լ���ù���������Ʒ�����ʵ���Ũ��_____________����2KMnO4 + 3H2SO4 + 5H2O2 == K2SO4 + 2MnSO4 + 5O2�� + 8H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ������˵������ȷ���ǣ� ��
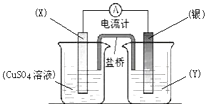
A. �缫X�IJ�����ͭ
B. �������ҺY����������Һ
C. ���缫Ϊ��ص������������ĵ缫��ӦΪ��Ag++e���TAg
D. �����е�������������ͭ��Һ���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£����1.92 g RO2ij��������Ϊ672 mL��
(1)�����庬���ӵ����ʵ���Ϊ__________��
(2)���������Է�������Ϊ__________��
(3)R�����ԭ������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�Ӧ3BrF3��5H2O===HBrO3��Br2��9HF��O2���У�����5 mol H2O��Ϊ��ԭ��ʱ������ԭ��BrF3�����ʵ���Ϊ(����)
A. 3 mol B. 2 mol C. ![]() mol D.
mol D. ![]() mol
mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУѧ��ʵ��С��Ϊ��֤��ͭ��ϡ���ᷴӦ����һ������������ͼ��ʾװ�ý���ʵ��(����װ�úͼг�װ�þ�����ȥ���������Ѽ��飬F�����ڹ��������˫��������)��
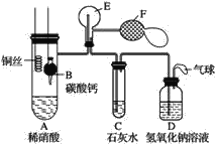
ʵ�����������Ϊ��
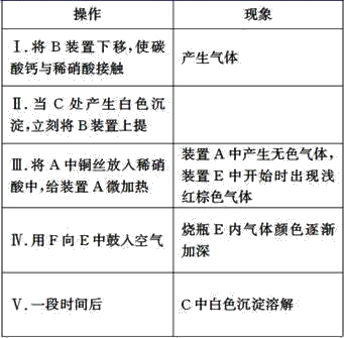
��1���������в�����������ӷ�Ӧ����ʽΪ__��
��2���������Ŀ����__��
��3��C�а�ɫ�����Ļ�ѧʽ��__���������е�C������ɫ����ʱ���̽�B�����ԭ����__��
��4����������װ��A������ɫ����Ļ�ѧ����ʽ��__��
��5����ƿE��������ɫ�����ԭ����__��
��6�����������������ԭ����(��ϻ�ѧ����ʽ˵��)__��
��7��Dװ�õ�������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��֤��±��Ԫ�صķǽ�����ǿ����ijС������ͼ��ʾװ�ý���ʵ��(�г���������ȥ���������Ѽ��)��
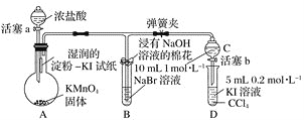
ʵ����̣�
��.���ɼУ�����a���μ�Ũ���ᡣ
��.��B��C�е���Һ����Ϊ��ɫʱ���н����ɼС�
��.��B����Һ�ɻ�ɫ��Ϊ�غ�ɫʱ���رջ���a��
��.����
(1)��֤������������ǿ�ڵ��ʵ��������________________________________________��
(2)B����Һ������Ӧ�����ӷ���ʽ��____________________________________________��
(3)Ϊ��֤���������ǿ�ڵ⣬���� �� �IJ�����������____________________________��
(4)���̢�ʵ���Ŀ����________________________________________________________��
(5)�ȡ��塢�ⵥ�ʵ�������������ԭ��ͬ����Ԫ�ش��ϵ��£�ԭ�Ӱ뾶��________���õ���������________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com