
碘化钡(BaI2·2H2O)是一种白色粉末,常用于制取其他含碘化合物。一种制备流程如下:
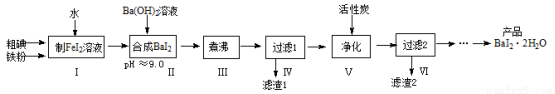
(1)步骤Ⅰ制FeI2溶液时,提高反应速率的可行措施有 (填序号)。
a.铁粉和碘粉用球磨机磨成细粉
b.增大n(铁粉)∶n(碘)的配料比
c.适当升高反应温度和搅拌速度
d.向反应器中加水至I2全部溶解
(2)步骤Ⅱ发生反应的化学方程式为 ;用pH试纸测定溶液pH的方法是 。
(3)步骤Ⅲ小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是 ;步骤V加入活性炭的目的是 。
(4)从过滤2所得滤液中获得BaI2·2H2O(溶解度曲线如右图所示)的方法是 。
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:实验题
某实验小组同学依据资料深入探究Fe3+在水溶液中的行为。
资料:i.Fe3+ 在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;
[Fe(H2O)6]3+发生如下水解反应:
[Fe(H2O)6]3+(几乎无色)+nH2O [Fe(H2O)6-n(OH)n]3-n(黄色)+nH3O+(n=0~6);
[Fe(H2O)6-n(OH)n]3-n(黄色)+nH3O+(n=0~6);
ii.[FeCl4(H2O)2]-为黄色。
【实验I】

【实验II】
分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。


图1 图2
Fe(NO3)3溶液透光率随温度变化曲线 FeCl3溶液透光率随温度变化曲线
(1)实验I中,试管②溶液变为无色的原因是 。
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是 。
(3)由实验II图1、2可知:加热时,溶液颜色 (填“变浅”、“变深”或“不变”)。
(4)由实验II,可以得出如下结论:
[结论一]FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O [Fe(H2O)6]3++4Cl-
[Fe(H2O)6]3++4Cl-
得出此结论的理由是 。
[结论二] 结论一中反应的ΔH (填“>0”或“<0”)。
(5)实验小组同学重新设计了一个实验证明(4)中结论一。实验方案:取试管①中溶液, (请描述必要的实验操作和现象)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南湖南省长沙市高三月考试卷三化学试卷(解析版) 题型:选择题
下列实验操作正确且能达到相应实验目的的是
实验目的 | 实验操作 | |
A | 称取2.0gNaOH固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
B | 在MgCl2、AlCl3溶液中分别通入氨气 | 比较镁、铝的金属性强弱 |
C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
D | 向NaBr溶液中滴入少量的氯水和CCl4,振荡、静置,溶液下层呈橙红色 | Cl-的还原性强于Br- |
查看答案和解析>>
科目:高中化学 来源:2017届河北辛集中学高三上理综测试三化学试卷(解析版) 题型:选择题
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解放的无水LiCl—KCl混合物受热熔融,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是

A.正极反应式:Ca+2Cl--2e-=CaCl2
B.放电过程中,Li+向负极移动
C.常溫时,在正负极间接上电流表或检流计,指针发生偏转
D.每转移0.1mol电子,理论上生成10.35g Pb
查看答案和解析>>
科目:高中化学 来源:2017届江苏省盐城市高三上学期期中化学试卷(解析版) 题型:填空题
亚硝酸盐与钴(Ⅲ)形成的一种配合物1Co(NH3)5NO2]Cl2的制备流程如下:

(1)Co2+基态核外电子排布式为 。
(2)配合物1Co(NH3)5Cl]Cl2中与Co3+形成配位键的原子为 (填元素符号);配离子 1Co(NH3)5NO2]2+的配体中氮原子的杂化轨道类型为 。
(3)与NO2-互为等电子体的单质分子为 (写化学式)。
(4)H2O2与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为 。
(5)亚硝酸盐在水体中可转化为强致癌物亚硝胺,亚硝胺NDMA的结构简式如图所示,1molNDMA分子中含有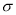 键的数目为 mol。
键的数目为 mol。

查看答案和解析>>
科目:高中化学 来源:2017届江苏省盐城市高三上学期期中化学试卷(解析版) 题型:选择题
制备5Ca(NO3)2·NH4NO3·10H2O的实验中,过滤出产品后,常温下另取母液(pH<1),向其中加入指定物质,反应后溶液中可大量存在的一组离子是
A.加入过量Na2CO3溶液:Na+、Ca2+、NH4+、NO3-、H+
B.加入适量NaHCO3溶液:Na+、Ca2+、NH4+、NO3-、HCO3-
C.加入适量NaOH溶液:Na+、Ca2+、NH4+、NO3-、OH-
D.加入过量FeSO4和稀硫酸:Fe2+、Fe3+、NH4+、Ca2+、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届江苏省盐城市高三上学期期中化学试卷(解析版) 题型:选择题
用实验室制溴苯的废催化剂FeBr3作原料,制取溴的苯溶液和无水FeCl3。下列设计能达到相应实验目的的是
A.用装置甲制取氯气
B.用装置乙氧化FeBr3溶液中的溴离子
C.用装置丙分液时先从下口放出水相,再从上口倒出有机相
D.用装置丁将分液后的水相蒸发至干,再灼烧制得无水FeCl3
查看答案和解析>>
科目:高中化学 来源:2017届江苏省徐州、宿迁、连云港、淮安四市高三11月模拟化学卷(解析版) 题型:选择题
真空碳热还 原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①Al2O3(s)+3C(s)=2Al(s)+3CO(g) △H1=1344.1kJ·mol-1
②2AlCl3(g)=2Al(s)+3Cl2(g) △H2=1169.2kJ·mol-1
③Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g) △H3=QkJ·mol-1
下列有关说法正确的是( )
A.反应①中化学能转化为热能
B.反应②中若生成液态铝则反应热应大于△H2
C.反应③中1molAlCl3(g)生成时,需要吸收174.9kJ的热量
D.该生产工艺中能循环利用的物质只有AlCl3
查看答案和解析>>
科目:高中化学 来源:2017届云南曲靖市高三上学期第三次月考化学试卷(解析版) 题型:选择题
如下图,CPAE是蜂胶的主要活性成分,也可由咖啡酸合成.下列说法不正确的是

A.咖啡酸分子中所有碳原子可能处在同一个平面上
B.1molCPAE与足量的溴水反应,最多消耗3molBr2
C.1mol苯乙醇在O2中完全燃烧,需消耗10molO2
D.1molCPAE与足量的NaOH溶液反应,最多消耗3molNaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com