
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。
请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为________,第一电离能最小的元素是________(填元素符号)。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是________(填化学式),呈现如此递变规律的原因是___________________。
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为________。另一种的晶胞如图二所示,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为________________________________________________g·cm-3(保留两位有效数字)。( =1.732)
=1.732)

图一 图二 图三
(4)D元素形成的单质,其晶体的堆积模型为________,D的醋酸盐晶体局部结构如图三,该晶体中含有的化学键是________(填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)向D的硫酸盐溶液中滴加过量氨水,观察到的现象是________。请写出上述过程的离子方程式:_________________________________________。
(1)  Cu
Cu
(2)HF>HI>HBr>HCl HF分子之间形成氢键使其熔沸点较高,HI、HBr、HCl分子之间只有范德华力,相对分子质量越大,范德华力越大
(3)sp2 3.5 (4)面心立方最密堆积 ①②③
(5)首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液 Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
【解析】 根据四种元素分别处于第一至第四周期,结合题中信息可确定A、B、C、D四种元素分别为H、C、Cl和Cu。(1)四种元素中电负性最大的是Cl,其基态原子的价电子数为7,价电子排布图为 ;结合第一电离能的变化规律,可知Cu的第一电离能最小。(2)卤化氢随着相对分子质量递增,其沸点升高,但HF分子间存在氢键,沸点最高,即沸点由高到低的顺序是HF>HI>HBr>HCl。(3)图一为平面分子,该物质碳原子采取sp2杂化;一个晶胞中含碳原子数为8×
;结合第一电离能的变化规律,可知Cu的第一电离能最小。(2)卤化氢随着相对分子质量递增,其沸点升高,但HF分子间存在氢键,沸点最高,即沸点由高到低的顺序是HF>HI>HBr>HCl。(3)图一为平面分子,该物质碳原子采取sp2杂化;一个晶胞中含碳原子数为8× +6×
+6× +4=8,该晶胞的密度为
+4=8,该晶胞的密度为 g·cm-3≈3.5 g·cm-3。(4)晶体Cu为面心立方最密堆积,结合图三醋酸铜晶体的局部结构可确定其晶体中含有极性键、非极性键和配位键。(5)硫酸铜溶液中加入氨水会产生蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,据此可写出反应的离子方程式。
g·cm-3≈3.5 g·cm-3。(4)晶体Cu为面心立方最密堆积,结合图三醋酸铜晶体的局部结构可确定其晶体中含有极性键、非极性键和配位键。(5)硫酸铜溶液中加入氨水会产生蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,据此可写出反应的离子方程式。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源:2014年高考化学指导冲关 第4练物质结构与元素周期律练习卷(解析版) 题型:选择题
X、Y、Z是原子序数依次增大的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是( )
A.原子半径:Z>Y>X
B.Z和X形成化合物的稳定性大于Z的同族元素与X形成化合物的稳定性
C.Na2Y2与水发生反应时,Na2Y2只作氧化剂
D.在CaX2、CaY2和CaZ2三种化合物中,阳离子与阴离子的个数比均为1∶2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第1练物质分类化学用语和常用计量练习卷(解析版) 题型:选择题
将5.1 g镁铝合金投入到500 mL 2.0 mol/L的盐酸中,金属完全溶解,再加入4.0 mol/L的NaOH溶液,若要生成的沉淀最多,则应加入NaOH溶液的体积是( )
A.200 mL B.250 mL C.425 mL D.560 mL
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第14练有机物的组成、结构和性质练习卷(解析版) 题型:填空题
姜黄素具有抗突变和预防肿瘤的作用,其合成路线如下:
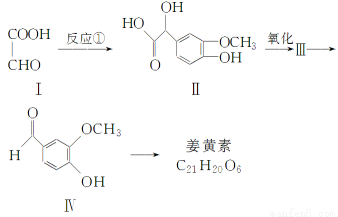
化合物Ⅰ可以由以下合成路线获得:

(1)有机物Ⅳ的分子式为________,含有官能团的名称为醚键和________。
(2)有机物Ⅴ的名称为________,其生成Ⅵ的化学方程式为(注明反应条件):_________________________________________________________________。
(3)写出一种符合下列条件的Ⅳ的同分异构体的结构简式
_______________________________________________________。
①苯环上的一硝基取代物有2种
②1 mol该物质水解,最多消耗3 mol NaOH
(4)反应①中反应物的原子利用率为100 %,请写出该反应的化学方程式
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第14练有机物的组成、结构和性质练习卷(解析版) 题型:选择题
乙烷在光照条件下与氯气发生取代反应,理论上得到的氯代物最多有几种 ( )
A.5种 B.6种 C.8种 D.9种
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第13练物质结构与性质练习卷(解析版) 题型:选择题
下列物质变化,只与范德华力有关的是( )
A.干冰熔化
B.乙酸汽化
C.乙醇与丙酮混溶
D.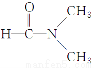 溶于水
溶于水
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第12练物质制备方案的设计与评价练习卷(解析版) 题型:填空题
工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计了如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理
①Al4C3与硫酸反应可生成CH4;
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程式____________________________________________________。
(2)实验装置(如图所示)
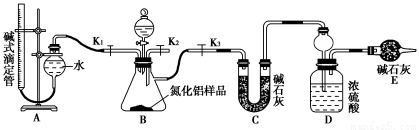
(3)实验过程
①连接实验装置,检验装置的气密性。称得D装置的质量为y g,滴定管的读数为a mL。
②称取x g AlN样品置于锥形瓶中;塞好胶塞,关闭活塞_____________,打开活塞______________,通过分液漏斗加入稀硫酸,与锥形瓶内物质充分反应。
③待反应进行完全后,关闭活塞_____________,打开活塞_____________,通过分液漏斗加入过量____________(填化学式),与烧瓶内物质充分反应。
④__________________(填入该步应进行的操作)。
⑤记录滴定管的读数为b mL,称得D装置的质量为z g,
(4)数据分析
①AlN的质量分数为___________________。
②若读取滴定管中气体的体积时,液面左高右低,则所测气体的体积_________________(填“偏大”、“偏小”或“无影响”)。
③Al4C3的质量分数为________。(该实验条件下的气体摩尔体积为Vm)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第11练化学实验基础知识练习卷(解析版) 题型:选择题
下列实验所用的试纸不能预先用蒸馏水湿润的是( )
A.用品红试纸检验SO2
B.用淀粉碘化钾试纸检验Cl2
C.用红色石蕊试纸检验氨气
D.用pH试纸测定某溶液的pH
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(三) (解析版) 题型:选择题
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图,下列判断正确的是( )
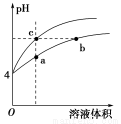
A.a、c两点溶液的导电能力相同
B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-)
C.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
D.a、b、c三点溶液水的电离程度a>b>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com