
含20.0 g NaOH的稀溶液与稀盐酸完全反应时,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
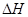 =
+28.7 kJ·mol-1
=
+28.7 kJ·mol-1
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
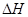 =
-28.7 kJ·mol-1
=
-28.7 kJ·mol-1
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
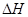 =
+57.4 kJ·mol-1
=
+57.4 kJ·mol-1
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
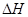 =
-57.4 kJ·mol-1
=
-57.4 kJ·mol-1
科目:高中化学 来源:江苏省金坛市第一中学2009届高三化学综合模拟 题型:021
|
设阿伏加德罗常数为NA.则下列说法正确的是 | |
A. |
常温常压下,20.0 g重水(D2O)中所含的电子数为10 NA |
B. |
1 cm3铁所含的铁原子数是ρ·NA/56(ρ是铁的密度,单位为g·cm-3) |
C. |
2.24 L CO2与足量的Na2O2反应,Na2O2转移的电子总数一定为0.1 NA |
D. |
常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源:2015届江苏省常州市高二期末考试化学试卷(解析版) 题型:选择题
某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Mg2+、Al3+、Clˉ。为确认该溶液组成进行如下实验:①取20.0 mL该溶液,加入25.0 mL 4.00 mol·L-1NaOH溶液,有白色沉淀、无剌激气味气体。过滤、洗涤、干燥,得沉淀1.16 g。再将滤液稀释至100 mL,测得滤液中c(OHˉ)为0.20 mol·L-1;②另取20.0 mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48 g。由此可得出关于原溶液组成的正确结论是
A.一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+
B.一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+
C.c (Clˉ) 为 4.00 mol·L-1,c (Al3+) 为1.00 mol·L-1
D.c (Mg2+) 为 1.00 mol·L-1,c(Na+ ) 为 0.50 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省高二1月学业水平模拟测试(四)化学试卷(解析版) 题型:选择题
某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Mg2+、Al3+、Clˉ。为确认该溶液组成进行如下实验:①取20.0 mL该溶液,加入25.0 mL 4.00 mol·L-1NaOH溶液,有白色沉淀、无剌激气味气体。过滤、洗涤、干燥,得沉淀1.16 g。再将滤液稀释至100 mL,测得滤液中c(OHˉ)为0.20 mol·L-1;②另取20.0 mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48 g。由此可得出关于原溶液组成的正确结论是
A.一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+
B.一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+
C.c (Clˉ) 为 4.00 mol·L-1,c (Al3+) 为1.00 mol·L-1
D.c (Mg2+) 为 1.00 mol·L-1,c(Na+ ) 为 0.50 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com