
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.48g正丁烷和10g异丁烷的混合物中共价键数目为13NA
B.3.4g羟基(-OH) 和3.4g氢氧根(OH-)均含有2NA个电子
C.7.8g 苯含有碳碳双键的数目为0.3NA
D.标准状况下,22.4L 由CHCl3和CH2Cl2组成的混合物中含有的分子数目为NA
【答案】A
【解析】
A.正丁烷的结构式为 ,1个正丁烷分子中,含有13个共价键;异丁烷的结构式为
,1个正丁烷分子中,含有13个共价键;异丁烷的结构式为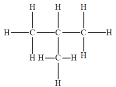 ,1个异丁烷分子中,含有13个共价键。正丁烷和异丁烷的相对分子式量相同,均为58,则48g正丁烷和10g异丁烷的混合物含有的分子的物质的量为1mol,每个分子中含有的共价键均为13个,则1mol的混合物含有的共价键的物质的量为13mol,数目为13NA,A正确;
,1个异丁烷分子中,含有13个共价键。正丁烷和异丁烷的相对分子式量相同,均为58,则48g正丁烷和10g异丁烷的混合物含有的分子的物质的量为1mol,每个分子中含有的共价键均为13个,则1mol的混合物含有的共价键的物质的量为13mol,数目为13NA,A正确;
B.1个-OH中含有9个电子,则3.4g-OH含有电子的物质的量为![]() ,其数目为1.8NA,B错误;
,其数目为1.8NA,B错误;
C.苯中不含碳碳双键,因此7.8g苯含有碳碳双键的数目为0NA,C错误;
D.在标况下,CHCl3和CH2Cl2均为液体,不能利用气体摩尔体积计算其物质的量,D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】![]() 时,向
时,向![]() 的NaOH溶液中逐滴加入某浓度的
的NaOH溶液中逐滴加入某浓度的![]() 溶液,滴定过程中,溶液的pH与滴入
溶液,滴定过程中,溶液的pH与滴入![]() 溶液的体积的关系如图所示,②点时NaOH溶液恰好被中和,则下列说法中,正确的是
溶液的体积的关系如图所示,②点时NaOH溶液恰好被中和,则下列说法中,正确的是![]()

A.该滴定过程应该选择甲基橙作为指示剂
B.点④所示溶液中存在:![]()
C.图中点①到点③所示溶液中,水的电离程度先减小后增大
D.点①所示溶液中存在:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 年,比利时人索尔维
年,比利时人索尔维![]()
![]() 用氨碱法生产碳酸钠.反应原理如下:
用氨碱法生产碳酸钠.反应原理如下:

![]() 时一些物质在水中的溶解度
时一些物质在水中的溶解度![]()
NaCl |
|
|
|
|
|
|
|
|
|

(1)氨碱法生成纯碱的原料是____________,可循环利用的物质有____________.
(2)饱和NaCl溶液通![]() 和
和![]() 能生成
能生成![]() 的原因有:____________/span>.
的原因有:____________/span>.
Ⅲ![]() 我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(3)生产中需向分离出![]() 后所得的溶液中加入NaCl固体并通入
后所得的溶液中加入NaCl固体并通入![]() ,在____________
,在____________![]() 填温度范围
填温度范围![]() 下析出____________
下析出____________![]() 填化学式
填化学式![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】增塑剂(又叫塑化剂)是一种增加塑料柔韧性、弹性等的添加剂,不能用于食品、酒类等行业。DBP(邻苯二甲酸二丁酯)是增塑剂的一种,可由下列路线合成:

已知以下信息:
①
![]()

②R2CHO+R2CH2CHO![]()
![]()
(-R1、-R2表示氢原子或烃基)
(1)A的结构简式 ______,D→E的反应类型 __________。
(2)DBP的分子式为 __________,D的结构简式是 ___________。
(3)由B和E以物质的量比1:2合成DBP的化学方程式: ________。
(4)写出同时符合下列条件的B的所有同分异构体结构简式 __________。
①能和NaHCO3溶液反应生成CO2;②能发生银镜反应
③能使FeCl3溶液发生显色反应;④苯环上含碳基团处于对位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌是制备荧光粉的原料之一。某实验室用炼锌厂的烟道灰(主要成分为:炭粉、ZnO、PbO、FeO、SiO2)制备皓矾(ZnSO4· 7H2O)的流程如下:

已知:ZnSO4易溶于水,难溶于乙醇。请回答下列问題:
(1)下列操作或描述正确的是 _________
A.“抽滤洗涤”时,将洗液与溶液I合并,有利于提高皓矾的产率
B.溶液I中含量较高的溶质有ZnSO4、PbSO4、FeSO4、H2SO4
C.重结晶时,需加少量稀盐酸抑制Zn2+水解
D. “洗涤干燥”时,可用95%的酒精作为洗涤剂
(2)如图安装抽滤装置,经过一系列操作完成抽滤。请选择合适的编号,按正确的搡作顺序补充完整:
在布氏漏斗中加入滤纸→_____ →_____→_______→________→确认抽干。__________

①转移固液混合物;②开大水龙头;③关闭水龙头;④微开水龙头;⑤加入少量蒸馏水润湿滤纸
(3)某同学设计了一个实验方案,证明晶体II中的杂质Fe3+含量低于晶体Ⅰ,请把该方案补充完整。_____ (填操作),分别加入2滴稀硝酸和6滴15%KSCN,________(填现象),证明晶体II中的杂质含量低于晶体I
(4)某同学称取28.700g研细的皓矾晶体(0.100mol), 置于坩埚中充分加热、冷却、称量,发现晶体失重13.100g。该同学分析认为,在加热失水过程中还发生副反应,该副反应可能的化学方程式为_____________
(5)将烟道灰在氧气中髙温灼烧后,再按上述流程操作,皓矾产率有明显提高,其原因是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,K=![]() =1.75×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是( )
=1.75×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是( )
A.向该溶液中加入一定量的硫酸,K增大
B.升高温度,K增大
C.向CH3COOH溶液中加入少量水,K增大
D.向CH3COOH溶液中加入少量氢氧化钠溶液,K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述不正确的是( )
A.电解精炼铜的阴极反应:Cu2+ +2e=Cu
B.常温时,0.1mol/L氨水的pH=11.1:NH3·H2O![]() +OH
+OH
C.醋酸钠使酚酞溶液变红:CH3COONa+H2O=CH3COOH+NaOH
D.由Na和Cl形成离子键的过程:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.水的电离方程式:H2O = H++OH-B.pH=7的溶液一定是中性溶液
C.升高温度,水的电离程度增大D.将稀醋酸加水稀释时,溶液中所有离子浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g) △H=-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO2+SO3(快); 4VO2+O2→2V2O5(慢),下列说法正确的是( )
2SO3(g) △H=-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO2+SO3(快); 4VO2+O2→2V2O5(慢),下列说法正确的是( )
A.反应速率主要取决于V2O5的质量B.VO2是该反应的催化剂
C.该反应逆反应的活化能大于198kJ/molD.升高温度,该反应的△H增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com