
����Ŀ���ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��ǻ�ѧ�ͼ�������ᷢչ������ľ���֮һ������ȡ�ϳɰ�ԭ�����Ĺ����У�������һЩ���ʣ���CO��ʹ�����ж�����ȥCO�Ļ�ѧ��Ӧ����ʽ(HAc��ʾ����)��Cu(NH3)2Ac + CO + NH3Cu(NH3)3(CO)Ac����ش��������⣺
(1)C��N��O�ĵ�һ�������ɴ�С��˳��Ϊ________��
(2)д����̬Cu+�ĺ�������Ų�ʽ_______��
(3)�����Cu(NH3)3(CO)Ac����ԭ�ӵ���λ��Ϊ______��
(4)д����CO��Ϊ�ȵ������������______��(��дһ��)
(5)��һ��������NH3��CO2�ܺϳɻ�������[CO(NH2)2]��1mol���ط����У���������ĿΪ______��
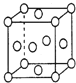
(6)��֪ͭ�ľ����ṹ��ͼ��ʾ������ͭ�ľ���������ͭԭ��������λ����Ϊ______��
���𰸡�N��O��C 1s22s22p63s23p63d10 4 CN����C22�� 7mol��7NA 1:3
��������
(1)һ����˵�ǽ�����Խǿ����һ������Խ������Ϊp����������ϵ���к�ǿ���ȶ��ԣ�
(2)ͭԭ�ӵĺ�������Ų�Ϊ1s22s22p63s23p63d104s1��
(3)���ݻ�����Ļ�ѧʽ�жϣ�һ��ͭ�������������������һ���ʻ����壬��4�����壻
(4)�ȵ�������ָ�۵�������ԭ������ͬ�ķ��ӡ����ӻ�ԭ���ţ�CO��10���۵��Ӻ�2��ԭ���ţ���������10�����Ӻ�2��ԭ�ӵ������Ӷ����ԣ�
(5)�����ӻ�����ʱ���ݵ��Ӷ������жϣ�
(6)���þ�̯�����㾧����ͭԭ�Ӹ�����ÿ����������һ��������ͭԭ�Ӿ��������ͭԭ������3��ÿ��������ͭԭ�ӱ�8������ռ�У��ݴ˼���ͭԭ����λ����
(1)һ����˵�ǽ�����Խǿ����һ�����ܴ�����O��N��C��������Ϊp����������ϵ���к�ǿ���ȶ��ԣ�N��p����������ǰ�����ģ�O��p���ʧȥһ�����Ӳ��ǰ�����ġ�����O��N����ʧȥ���ӣ���һ�������ɴ�С��˳��ΪN��O��C��
(2)ͭԭ�ӵĺ�������Ų�Ϊ1s22s22p63s23p63d104s1����һ��ͭ���ӵĺ�������Ų�Ϊ1s22s22p63s23p63d10��
(3)һ��ͭ�������������������һ���ʻ����壬��4�����壻
(4) �ȵ�������ָ�۵�������ԭ������ͬ�ķ��ӡ����ӻ�ԭ���ţ�CO��10���۵��Ӻ�2��ԭ���ţ���������10�����Ӻ�2��ԭ�ӵ������Ӷ����ԣ���CN��C22��ҲΪ14�����ӣ�
(5)��ԭ���γ���3��������ͬʱ����һ�Թµ��ӣ����Ӷ���Ϊ3+1=4�����ӻ���ʽΪsp3����������ĿΪ3��ÿ���ǰ�������������Ŀ2��һ���������к���������ĿΪ3+2��2=7����ÿĦ�������к�����������ĿΪ7NA����
(6)ÿ��������ͭԭ�Ӹ���=8��![]() +6��
+6��![]() =4����ͭ�ľ����У������ϵ�ͭԭ�ӱ�8������ռ�У�ÿ����������һ��������ͭԭ�Ӿ��������ͭԭ������3��ÿ�����ϵ�ͭԭ�ӱ�2������ռ�У���������λ����3��8��
=4����ͭ�ľ����У������ϵ�ͭԭ�ӱ�8������ռ�У�ÿ����������һ��������ͭԭ�Ӿ��������ͭԭ������3��ÿ�����ϵ�ͭԭ�ӱ�2������ռ�У���������λ����3��8��![]() =12������ͭ�ľ���������ͭԭ��������λ����=4��12=1��3��
=12������ͭ�ľ���������ͭԭ��������λ����=4��12=1��3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ϵ��ȷ����( )
A. �е㣺���飾2��2-�������飾2��3-�������飾����
B. �ܶȣ�CCl4��CHCl3��H2O����
C. �����������������飾���飾��ϩ����Ȳ����
D. ������������ȼ�պ�O2�����������飾��ϩ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼ����ؿ���������������Ĺ�����Դ��һ���ȼ����صĻ����ṹ��ͼ��ʾ��������Ϊ����ʵ���ˮLiCl��KCl������������ں�ؼ���˲��������ܡ��õ���ܷ�ӦΪPbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb�������й�˵����ȷ����
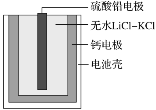
A.�ŵ�����У�Cl-�������ƶ�
B.������Ӧʽ��PbSO4+2e��=Pb+SO42��
C.��Ӧÿת��0.1mol���ӣ���������������4g Ca
D.����ʱ��������������ϵ�������ָ�뷢��ƫת
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ�������йظ����ʵ�˵����ȷ���ǣ� ��
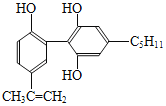
A.�÷����е�����ԭ���п��ܹ�ƽ��
B.�������뱽������ͬϵ���FeCl3��Һ����ɫ
C.����KMnO4(H+)��Һ���۲���ɫ��ȥ��˵���ṹ��һ�����ڲ�����̼̼��
D.1mol�����ʷֱ���Ũ��ˮ��H2��Ӧʱ������ĵ�Br2��H2�ֱ�Ϊ4mol��7mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���屽��һ����Ҫ����ԭ�ϣ�ʵ�����Ʊ��屽�ķ�Ӧװ����ͼ��ʾ���й��������£�
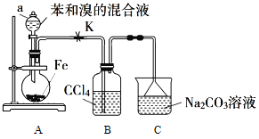
�� | �� | �屽 | |
��Է������� | 78 | 160 | 157 |
�ܶ�/gcm-3 | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
ˮ���ܽ�� | �� | �� | �� |
�����кϳɲ���ش����⣺
��1������a������Ϊ___��
��2����Aװ���м���7.8mL��ˮ��������Һ̬���������м��ʵ��ʱװ��B�п��ܵ�����Ϊ___��װ��C��������___��
��3����Ӧ��ֺ�ȡAװ���з�ӦҺ���������в�������ᴿ��
�������м�������___�����Լ����ƣ���Ȼ��___����������ƣ���ȥδ��Ӧ����м��
����Һ������ˮ��l0%��NaOH��Һ��ˮϴ�ӡ�NaOH��Һϴ�ӵ�������___��
����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����ˡ�
��4�������Ϸ���������屽�л�����һ���������ʣ�Ҫ��һ���ᴿ�����������ڸ��ᴿ������û��ʹ�õ�����___(������ȷѡ��ǰ����ĸ)��
A. B.
B.![]() C. D.
C. D.
��5�����յõ���Ʒ5.5mL����ʵ��IJ�����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ֱ���ͬϵ��0.1mol ����������������ȫȼ�գ��������ĸ�����������ͨ��Ũ���������������Һ��ʹŨ��������9g������������Һ����35.2g��ʵ���пɸ��ݺ˴Ź������ף�PMR���Ϲ۲쵽��ԭ�Ӹ����ķ�ֵ�����ȷ���л���Ľṹ���˺��б������л����PMR���Ϸ�������ȶ�ǿ�Ƚ������֣����Ƿֱ�Ϊ����3��1��1��1��1��2��6��3��2��3��2��2��2��1����ֱ��ƶϳ����Ӧ�Ľṹ����_______����_________________����___________����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ��������������W��ԭ��������Z��ԭ��������һ�룬W��X��Y����Ԫ���γɵĻ�����M�ṹ��ͼ��ʾ������������ȷ����
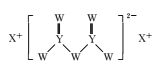
A.ԭ�Ӱ뾶��Z>Y>W
B.������M��W��ԭ������8�����ȶ��ṹ
C.��Ӧ���ʵ��۵㣺X>Z>Y
D.Z���������Ӧ��ˮ����Ϊǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪P4���ʵĽṹ���£�P4�� KOH ��Һ�еı仯�ǣ�P4 + 3KOH + 3H2O = 3KH2PO2 + PH3 ��������˵����ȷ���ǣ� ��
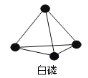
A.���� PH3���������е�ԭ�ӿ��ܹ�ƽ��
B.31gP4���� 1.5NA�� P P ��
C.���Ԫ�صĵ縺�Դ�С˳��P > O > H > K
D.P4�� P ԭ��Ϊ sp2�ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���Ҷ���(HOOC��COOH���ɼ�дΪH2C2O4)���׳Ʋ��ᣬ157��ʱ��ʼ�ֽ⡣
(1)̽�����������
25�� H2C2O4 K1��5.4��10-2��K2��5.4��10-5��H2CO3 K1��4.5��10-7��K2��4.7��10-11
���л�ѧ����ʽ������ȷ����___��
A��H2C2O4+![]() =
=![]() +
+![]() B��
B��![]() +
+![]() =
=![]() +
+![]()
C��2![]() +CO2+H2O=2
+CO2+H2O=2![]() +
+![]() D��H2C2O4+
D��H2C2O4+![]() =
=![]() +H2O+CO2��
+H2O+CO2��
(2)̽������ֽ����
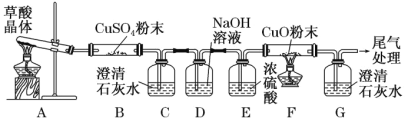
ʵ���й۲쵽 B �� CuSO4 ��ĩ������C �г���ʯ��ˮ����ǣ�D �������� ___�� ֤���� CO �������ɵ�������______��
(3)̽�������Ի�ѧ��Ӧ���ʵ�Ӱ��
�ڼס�����֧�Թ��и����� 4 mL 0.01 mol��L-1 ���� KMnO4 ��Һ�� 2 mL 0.1 mol��L-1H2C2O4 ��Һ���������Թ��м���һ���ƶ���� MnSO4 ���壬ҡ�ȡ���д����
��Ӧ���� | ��_______ |
ʵ����� | ��______ |
�Թ��з�����Ӧ�����ӷ���ʽ | ��______ |
(4)������ KMnO4 ��Һ�ζ� Na2C2O4������ Na2C2O4 �Ĵ��ȡ�
ʵ�鲽�裺ȷ��ȡ 2.0 g Na2C2O4 ���壬��� 100 mL ��Һ��ȡ�� 20.00 mL ����ƿ
��KMnO4 ��ҺӦװ��_________ �ζ����С�(������ʽ��������ʽ��)
��Na2C2O4 �Ĵ�����_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com