
【题目】以煤、天然气和生物质为原料制取有机化合物日益受到重视。E是两种含有碳碳双键的酯的混合物。相关物质的转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):

请回答:
(1) A→B的反应类型________,C中含氧官能团的名称________。
(2) C与D反应得到E的化学方程式________。
(3) 检验B中官能团的实验方法________。
【答案】氧化反应 羧基 ![]() +CH2=CHCOOH
+CH2=CHCOOH![]()
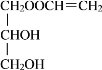 +H2O
+H2O ![]() +CH2=CHCOOH
+CH2=CHCOOH![]()
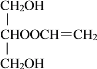 +H2O 加过量银氨溶液,加热,出现银镜,说明有醛基;用盐酸酸化,过滤,滤液中加入溴水,若溴水褪色,说明有碳碳双键
+H2O 加过量银氨溶液,加热,出现银镜,说明有醛基;用盐酸酸化,过滤,滤液中加入溴水,若溴水褪色,说明有碳碳双键
【解析】
B到C发生氧化反应,醛基被氧化成羧基,C为![]() ,油脂在酸性条件下水解得到高级脂肪酸和甘油,结合D的分子式,可知D为甘油
,油脂在酸性条件下水解得到高级脂肪酸和甘油,结合D的分子式,可知D为甘油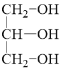 ,C和D发生酯化反应得到E,结合E的分子式可知-OH和-COOH发生1:1酯化,混合物E的结构简式为
,C和D发生酯化反应得到E,结合E的分子式可知-OH和-COOH发生1:1酯化,混合物E的结构简式为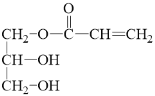 和
和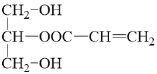 。
。
(1)根据分子组成的变化,即去氢加氧,A到B的反应类型为氧化反应,C中的含氧官能团为羧基。
(2)由上分析混合物E的结构简式,可知C和D的酯化反应得到两种有机产物,因而化学方程式分别为![]() +CH2=CHCOOH
+CH2=CHCOOH![]()
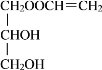 +H2O和
+H2O和![]() +CH2=CHCOOH
+CH2=CHCOOH![]()
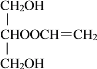 +H2O。
+H2O。
(3)B中含有碳碳双键和醛基,两者都易被氧化,其中醛基能被弱氧化剂氧化,因而需要先检验醛基,可采用银氨溶液检验,注意这里需要加过量的银氨溶液以便将醛基全部氧化,然后用盐酸酸化,原因在于银氨溶液呈碱性,能和溴水反应,然后将过滤后的滤液加入溴水,观察现象。因而答案为加过量银氨溶液,加热,出现银镜,说明有醛基;用盐酸酸化,过滤,滤液中加入溴水,若溴水褪色,说明有碳碳双键。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是( )
A.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
B.78g ![]() 中含有双键数为3NA
中含有双键数为3NA
C.17g![]() 中含有的电子数为9NA
中含有的电子数为9NA
D.常温常压下,1 L甲醛气体所含的分子数小于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D,A元素的原子最外层电子数是内层电子数的两倍,B为地壳中含量最多的元素,C是原子半径最大的短周期主族元素,C与D形成的离子化合物CD是常用的调味品。填写下列空白:
(1)A的基态原子的电子排布式为_________________;
(2)C元素在周期表中的位置是____________________
(3)B、C组成的一种化合物与水发生反应生成气体,其化学方程式为:_________。
(4)如图所示,电解质a溶液为含有CD的饱和溶液。X为石墨电极,Y为铁电极,接通直流电源。
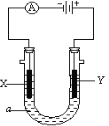
X电极的电极反应式为___________,电解池总反应的离子方程式为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制100mL1.0 mol/L Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4,溶于100mL水中
②将32.2g Na2SO410H2O溶于少量水中,再用水稀释至100 mL
③将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
A.①②B.②③C.①③D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH-△H>0,下列叙述正确的是( )
A. 向平衡体系中加入水,平衡正向移动,c (H+)增大
B. 将水加热,Kw增大,pH不变
C. 向水中加入少量硫酸氢钠固体,  增大
增大
D. 向水中加入少量NaOH固体,平衡正向移动,c(H+)降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一密闭容器中发生如下可逆反应:![]() ;
;![]() 若起始时E浓度为a
若起始时E浓度为a![]() ,F、G浓度均为0,达平衡时E浓度为0.5a
,F、G浓度均为0,达平衡时E浓度为0.5a![]() ;若E的起始浓度改为2a
;若E的起始浓度改为2a![]() ,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
A.升高温度时,正反应速率加快、逆反应速率减慢
B.若![]() ,容器体积保持不变,新平衡下E的体积分数为
,容器体积保持不变,新平衡下E的体积分数为![]()
C.若![]() ,容器体积保持不变,新平衡下F的平衡浓度小于
,容器体积保持不变,新平衡下F的平衡浓度小于![]()
![]()
D.若![]() ,容器压强保持不变,新平衡下E的物质的量为amol
,容器压强保持不变,新平衡下E的物质的量为amol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)![]() xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )
xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )

A. 若x=3,达到平衡后A的体积分数关系为:![]()
B. 若x<3,C的平衡浓度关系为:c(M)<c(N)
C. 若x>3,达到平衡后B的转化率关系为:![]()
D. x不论为何值,平衡时M、N中的平均相对分子质量都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市售盐酸试剂瓶标签上的部分信息如下:

(1)该盐酸的物质的量浓度为__________ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中c(HCl)=____mol·L-1。
(3)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是____ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图,判断下列叙述中正确的是
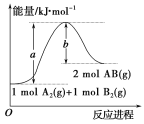
A.该反应的活化能是b kJ/mol
B.该反应热ΔH=+(a-b)kJ/mol
C.该反应中反应物的总能量高于生成物的总能量
D.1molA2(g)和1molB2(g)的能量总和是akJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com