
��֪A��BΪ�����Ľ������ʣ�C��DΪ�����ķǽ������ʣ��ס��ҡ���Ϊ���ֳ����Ļ��������֮����ת����ϵ����ͼ��ʾ(���ֲ��P��Ӧ����û���г�)��
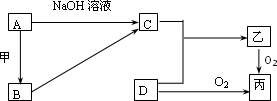
(1)��������ѧ��ѧ�г����ĺ���ɫ��ĩ״���壬��A�����һ�������·�Ӧ����B�Ļ�ѧ����ʽΪ________��A��NaOH��Һ��Ӧ�����ӷ���ʽΪ________��
(2)��ͨ��DΪ��̬���������г�������ζ��ˮ��Һ�������ԣ�����һ�ִ�����Ⱦ��д̼�����ζ����д�������ҷ�Ӧ�Ļ�ѧ����ʽ________��
(3)���ҵ�ˮ��Һ�������ԣ���������ũҵ���ʣ�DΪ�����к������ĵ��ʣ�д����ҵ������C��D��Ӧ�Ʊ��ҵĻ�ѧ����ʽ________��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| c(CH3OH) |
| c(CO)��c2(H2) |
| c(CH3OH) |
| c(CO)��c2(H2) |
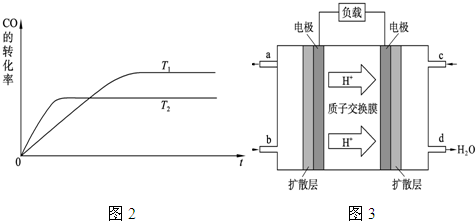
| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
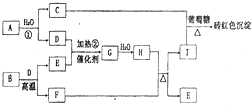 ��2011?֣�ݶ�ģ����ͼΪ����A?I��ת����ϵ�����ַ�Ӧ�������û���г���������BΪij��м�����Ҫ�ɷ֣�����һϵ�з�Ӧ�ɵõ�E��F��D��E������Ϊ���壬D��FΪ�������ʣ�
��2011?֣�ݶ�ģ����ͼΪ����A?I��ת����ϵ�����ַ�Ӧ�������û���г���������BΪij��м�����Ҫ�ɷ֣�����һϵ�з�Ӧ�ɵõ�E��F��D��E������Ϊ���壬D��FΪ�������ʣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�



| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ȼ��һ��Ҫ�û�ȥ��ȼ | B����֪��Ԫ��λ�����ڱ��е�4���ڵڢ�A�壬������������Ա�ƫ����ǿ�������صĽ����Ա����� | C��2013��ŵ������ѧ��������λ������ѧ�ң��Ա���������Ƴ���߶ȸ��ӻ�ѧϵͳģ�ͣ�����ͳ��ѧʵ��ᵽ���������磮��һ���������ʵ�����۵Ļ�ѧϵͳģ�ͣ�Ϊ��ȫ���˽ⲢԤ�⻯ѧ��Ӧ���̵춨�˻��� | D�����ʵ�ʹ����Ч�������ũ����IJ����������ĵ��ʿɷ�Ϊ�̬���ʺ���̬���ʣ������κ����ض�������̬���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
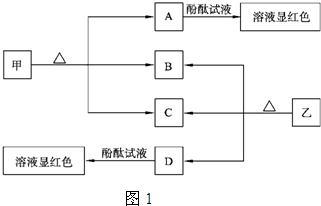
(08�㽭������ʮ��У����)��֪����ס�E��I��F��Ϊ�����ĵ��ʣ�����E�ڳ�����Ϊ��̬��GΪ��ɫ��״�����������ܽ������ᣬ�����ܽ�������������Һ��A�ڳ�����Ϊ��̬����������ȫ��Ӧʱ���������1:2��W�������ִ��ڲ�ͬ�����ڵ�Ԫ����ɵĻ������ˮ��Ӧ����A��Gʱ�Ļ�ѧ������֮��Ϊ1:3:3:1��������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�IJ���δȫ����ʾ�����Իش��������⣺ 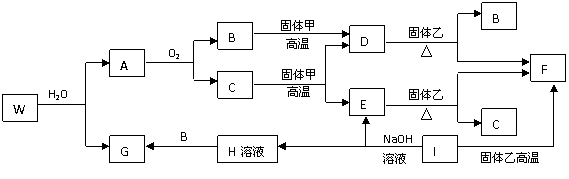
��1��B�ĵ���ʽΪ �������ҵĻ�ѧʽ������ ��
��2������ת���У���C��E ��D��F ��E��F ��I��F ��I��E ��A��B ���������û���Ӧ���ǣ�����ţ� ��
��3��д��W��ˮ��Ӧ�Ļ�ѧ����ʽ____________________________________________,
I��NaOH��Һ��Ӧ�����ӷ���ʽ________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com