
��һ������ܱ������У��������·�Ӧ��
CO2(g) + H2(g) 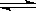 CO(g) + H2O(g),
CO(g) + H2O(g),
��ƽ�ⳣ���˺��¶�t�Ĺ�ϵ���£�
|
t�� |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1) K�ı���ʽΪ��������������������
(2) �÷�ӦΪ�������� ��Ӧ�������ȡ����ȡ���
(3) ���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬������
A��������ѹǿ���䡡�� B�����������COŨ�Ȳ���
C��v(H2)�� = v(H2O)�桡�� D��c(CO2) = c(CO)
(4)��830��ʱ������ʼŨ��c(CO)Ϊ1mol��L��1��c(H2O)Ϊ1mol��L��1����Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ ��
��1��K= 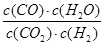
��2�� ����
��3��B C
��4��50%
��������
���������(1) K�ı���ʽΪK= 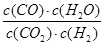 ��(2)����֪�����¶�Խ�ߣ�KԽ�����Ը÷�ӦΪ���ȷ�Ӧ��(3) ���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬������Ϊ���������COŨ�Ȳ��䡢v(H2)�� = v(H2O)�棬��BC��ȷ��A������Ϊ��Ӧһֱ����ѹǿ���䣬����������Ϊ�ﵽƽ��״̬�����ݣ�DҲ����c(CO2) = c(CO)ֻ��ij�������е�����������������Ϊ�ﵽƽ��״̬�����ݣ�(4)�ɱ�����֪������830��ʱ��KΪ1������
��(2)����֪�����¶�Խ�ߣ�KԽ�����Ը÷�ӦΪ���ȷ�Ӧ��(3) ���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬������Ϊ���������COŨ�Ȳ��䡢v(H2)�� = v(H2O)�棬��BC��ȷ��A������Ϊ��Ӧһֱ����ѹǿ���䣬����������Ϊ�ﵽƽ��״̬�����ݣ�DҲ����c(CO2) = c(CO)ֻ��ij�������е�����������������Ϊ�ﵽƽ��״̬�����ݣ�(4)�ɱ�����֪������830��ʱ��KΪ1������
K= 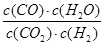 =1����ʼŨ��c(CO)Ϊ1mol��L��1��c(H2O)Ϊ1mol��L��1��ƽ��ʱ�������ʵĵ�Ũ��Ϊa����1-a����1-a��/��a��a��=1������aΪ0.5mol��L��1������CO��ת����Ϊ50%��
=1����ʼŨ��c(CO)Ϊ1mol��L��1��c(H2O)Ϊ1mol��L��1��ƽ��ʱ�������ʵĵ�Ũ��Ϊa����1-a����1-a��/��a��a��=1������aΪ0.5mol��L��1������CO��ת����Ϊ50%��
���㣺��ѧƽ��
���������⿼���˻�ѧƽ���֪ʶ���Ǹ߿�������ص㣬����Ƚ����ס�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ������ܱ������У��������·�Ӧ�� CO2(g)+ H2(g) CO(g) + H2O(g),��ƽ�ⳣ���˺��¶�t�Ĺ�ϵ���£�
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1) K�ı���ʽΪ��������������������
(2) �÷�ӦΪ����������Ӧ�������ȡ����ȡ���
(3) ���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬������
����������ѹǿ���䡡�� �£����������COŨ�Ȳ���
�ã�v(H2)�� = v(H2O)�� ���� D��c(CO2) =c(CO)��
(4) ��830��ʱ������ʼŨ��c(CO)Ϊ1mol��L��1��c(H2O)Ϊ1mol��L��1����Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ɽ��ʡ���������ѧУ�߶���ѧ�����п��Ի�ѧ�������Ծ� ���ͣ������
��һ������ܱ������У��������·�Ӧ�� CO2(g)
+ H2(g) 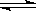 CO(g) + H2O(g),��ƽ�ⳣ���˺��¶�t�Ĺ�ϵ���£�
CO(g) + H2O(g),��ƽ�ⳣ���˺��¶�t�Ĺ�ϵ���£�
|
t�� |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1) K�ı���ʽΪ��������������������
(2) �÷�ӦΪ����������Ӧ�������ȡ����ȡ���
(3) ���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬������
����������ѹǿ���䡡�� �£����������COŨ�Ȳ���
�ã�v(H2)�� = v(H2O)�� ���� D��c(CO2) = c(CO)��
(4) ��830��ʱ������ʼŨ��c(CO)Ϊ1mol��L��1��c(H2O)Ϊ1mol��L��1����Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com