
0.01mol氯化铬(CrCl3•6H2O)在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此氯化铬最可能是( )
|
| A. | [Cr(H2O)6]Cl3 | B. | [Cr(H2O)5Cl]Cl2 |
|
| C. | [Cr(H2O)4Cl2]Cl•2H2O | D. | [Cr(H2O)3Cl3]•3H2O |
考点:
配合物的成键情况.
专题:
化学键与晶体结构.
分析:
氯化铬(CrCl3•6H2O)中的阴离子氯离子能和银离子反应生成氯化银沉淀,注意配体中的氯原子不能和银离子反应,根据氯化铬(CrCl3•6H2O)和氯化银物质的量的关系式计算氯离子个数,从而确定氯化铬(CrCl3•6H2O)的化学式.
解答:
解:根据题意知,氯化铬(CrCl3•6H2O)和氯化银的物质的量之比是1:2,根据氯离子守恒知,一个氯化铬(CrCl3•6H2O)化学式中含有2个氯离子,剩余的1个氯离子是配原子,所以氯化铬(CrCl3•6H2O)的化学式可能为[Cr(H2O)5Cl]Cl2•H2O,故选B.
点评:
本题考查了配合物的成键情况,难度不大,注意:该反应中,配合物中配原子不参加反应,只有阴离子参加反应,为易错点.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
下列解释实验事实的离子方程式正确的是( )
A. 纯碱溶液显碱性的原因:CO32﹣+2H2O⇌H2CO3+2OH﹣
B. 氯化铁溶液腐蚀铜线路板Cu+Fe3+=Cu2++Fe2+
C. 稀硫酸与氢氧化钡溶液恰好中和:Ba2++OH﹣+H++SO42﹣=BaSO4↓+H2O
D. 氯气溶于水:Cl2+H2O=H++Cl﹣+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列叙述中正确的是( )
①106g Na2CO3晶体中的离子总数大于3NA
②标准状况下,16g O3和O2混合气体中含有的氧原子数为NA
③将0.1mol NaCl全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为0.1NA
④1mol N2和3mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA.
|
| A. | ①② | B. | ②④ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂.下列对于过氧化钙(CaO2)的叙述错误的是( )
|
| A. | CaO2具有氧化性,对面粉可能具有增白作用 |
|
| B. | CaO2中阴阳离子的个数比为1:1 |
|
| C. | CaO2和水反应时,每产生1mol O2转移电子4mol |
|
| D. | CaO2和CO2反应的化学方程式为:2CaO2+2CO2=2CaCO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
粘合剂M的合成路线如图所示: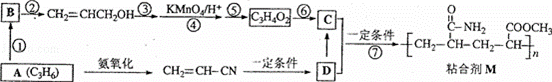
完成下列填空:
1)写出A和B的结构简式.
A B
2)写出反应类型.反应⑥ 反应⑦
3)写出反应条件.反应② 反应⑤
4)反应③和⑤的目的是 .
5)C的具有相同官能团的同分异构体共有 种.
6)写出D在碱性条件下水的反应方程式. .
查看答案和解析>>
科目:高中化学 来源: 题型:
对Na、Mg、Al的有关性质的叙述正确的是( )
|
| A. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | B. | 第一电离能:Na<Mg<Al |
|
| C. | 电负性:Na>Mg>Al | D. | 还原性:Na>Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NH3分子可与Cu2+形成配合物离子[Cu(NH3)4]2+,则除去硫酸铜溶液中少量硫酸可选用的试剂是( )
|
| A. | NaOH | B. | NH3 | C. | BaCl2 | D. | Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)⇌2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表,下列说法正确的是()
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
A. 反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(L•min)
B. 其他条件不变,降低温度,反应达到新平衡前v(逆 )>v(正)
)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)键线式 表示的分子式 ;名称是 .
表示的分子式 ;名称是 .
(2)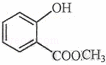 中含有的官能团的名称为 .
中含有的官能团的名称为 .
(3)丁基的4个结构简式为 、 , 、 , 、
(4)含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、 、 、 、尾接管、 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com