
粘合剂M的合成路线如图所示: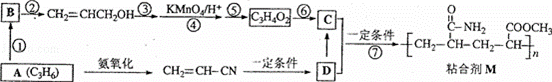
完成下列填空:
1)写出A和B的结构简式.
A B
2)写出反应类型.反应⑥ 反应⑦
3)写出反应条件.反应② 反应⑤
4)反应③和⑤的目的是 .
5)C的具有相同官能团的同分异构体共有 种.
6)写出D在碱性条件下水的反应方程式. .
考点:
有机物的合成;有机物分子中的官能团及其结构;同分异构现象和同分异构体;有机化学反应的综合应用.
专题:
压轴题.
分析:
根据合成路线图,A为C3H6和后续反应,应为CH3CH=CH2;A转化为B后,B可以继续生成CH2=CHCH2OH,说明B是卤代烃,即
CH2=CHCH2Cl(CH2=CHCH2Br),在碱性条件下加热水解生成CH2=CHCH2OH,被氧化为CH2=CHCOOH,由于CH2=CHCH2OH直接氧化,会导致C=C和﹣OH都能被酸性高锰酸钾氧化,则③应为加成反应生成CH3﹣CHClCH2OH,氧化后生成CH3﹣CHClCOOH,然后水解生成CH2=CHCOOH,由黏合剂M可知D为CH2=CHCO﹣NH2,C为CH2=CHCOOCH3,说明CH2=CH﹣CN在一定条件下 ,
,
CH2=CHCOOH与甲醇发生酯化反应生成CH2=CHCOOCH3,CH2=CHCOOCH3和 发生加聚反应生成黏合剂M,结合物质的结构和性质解答该题.
发生加聚反应生成黏合剂M,结合物质的结构和性质解答该题.
解答:
解:根据合成路线图,A为C3H6和后续反应,应为CH3CH=CH2;A转化为B后,B可以继续生成CH2=CHCH2OH,说明B是卤代烃,即CH2=CHCH2Cl(CH2=CHCH2Br),在碱性条件下加热水解生成CH2=CHCH2OH,被氧化为CH2=CHCOOH,由于CH2=CHCH2OH直接氧化,会导致C=C和﹣OH都能被酸性高锰酸钾氧化,则③应为加成反应生成CH3﹣CHClCH2OH,氧化后生成CH3﹣CHClCOOH,然后水解生成CH2=CHCOOH,由黏合剂M可知D为CH2=CHCO﹣NH2,C为CH2=CHCOOCH3,说明CH2=CH﹣CN在一定条件下 ,
,
CH2=CHCOOH与甲醇发生酯化反应生成CH2=CHCOOCH3,CH2=CHCOOCH3和 发生加聚反应生成黏合剂M,则
发生加聚反应生成黏合剂M,则
1)由以上分析可知,A为:CH3CH=CH2,B为CH2=CHCH2Cl(CH2=CHCH2Br),
故答案为:CH3CH=CH2;CH2=CHCH2Cl(CH2=CHCH2Br);
2)根据路线图中的变化,可知反应⑥是酯化反应;反应⑦是加聚反应,
故答案为:酯化反应;加聚反应;
3)反应②是卤代烃水解,其反应条件为:NaOH/H2O,加热;反应⑤为消去反应,条件是:NaOH/C2H5OH,
加热故答案为:NaOH/H2O,加热;NaOH/C2H5OH,加热;
4)由于CH2=CHCH2OH直接氧化,会导致C=C和﹣OH都能被酸性高锰酸钾氧化,反应过程中③和⑤的目的是保护碳碳双键,
故答案为:保护碳碳双键;
5)C是CH2=CH﹣COOCH3,含有C=C和﹣COO﹣,其含有相同官能团的同分异构体有:HCOOCH2CH=CH2、HCOOCH=CHCH3、HCOOC(CH3)=CH2、CH3COOCH=CH2等4种,
故答案为:4种;
6) 含有肽键,在碱性条件下生成﹣COONa和NH3,反应的化学方程式为
含有肽键,在碱性条件下生成﹣COONa和NH3,反应的化学方程式为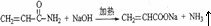 ,
,
故答案为: .
.
点评:
此题考查了有机合成知识,题目难度中等,解答有机合成题时:首先要判断待合成有机物的类别、带有何种官能团,然后结合所学知识或题给新信息,分析得出官能团的引入、转换、保护或消去的方法,找出合成该有机物的关键和题眼.
①顺推法:研究原料分子的性质,找出合成所需的直接或间接的中间产物,逐步推向待合成的有机化合物.
②逆推法:从目标分子入手,分析目标有机物的结构特点,找出合成所需的直接或间接的中间产物,逐步推向已知原料,再设计出合理的线路.
③综合法:既从原料分子进行正推,也从目标分子进行逆推法,同时通过中间产物衔接两种方法得出最佳途径的方法.


科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是( )
A. Al3+的结构示意图:
B. 水的电子式:
C. 乙烯的结构简式:CH2CH2
D. 含有7个中子的碳原子: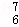 C
C
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl﹣ | |
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | / | Cl2 |
|
| A. | 表中①组反应可能有一种或两种元素被氧化 |
|
| B. | 氧化性强弱比较:KClO3>Cl2>Fe3+>Br2 |
|
| C. | 表中②组反应的离子方程式是2MnO4﹣+3H2O2+6H+═2Mn2++4O2↑+6H2O |
|
| D. | 表中③组反应的还原产物是KCl,电子转移数目是6e﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是( )
①FeBr2、氯水;
②NaHCO3、Ca(OH)2;
③NaHSO4、Ba(OH)2;
④AlCl3、氨水;
⑤AgNO3、氨水;
⑥Na2CO3、盐酸;
⑦NaAlO2、盐酸;
⑧FeCl3、NaOH.
|
| A. | ①②③④ | B. | ④⑤⑥⑧ | C. | 除④⑧外 | D. | ⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
0.01mol氯化铬(CrCl3•6H2O)在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此氯化铬最可能是( )
|
| A. | [Cr(H2O)6]Cl3 | B. | [Cr(H2O)5Cl]Cl2 |
|
| C. | [Cr(H2O)4Cl2]Cl•2H2O | D. | [Cr(H2O)3Cl3]•3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
|
| A. | X与Y形成化合物时,X可以显负价,Y显正价 |
|
| B. | 第一电离能可能Y小于X |
|
| C. | 最高价含氧酸的酸性:X对应的酸的酸性弱于Y对应的酸的酸性 |
|
| D. | 气态氢化物的稳定性:HmY小于HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:
在透明的碱性溶液中,能够大量共存的离子组是()
A. Fe3+、Ag+、NO3﹣、C1﹣ B. Mg2+、 NH4+、NO3﹣、C1﹣
NH4+、NO3﹣、C1﹣
C. Na+、K+、CO32﹣、NO3﹣ D. A13+、Na+、MnO4﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法.其方法是让极少量的(10﹣9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子.如C2H6离子化后可得到C2H6+、C2H5+、C2H4+…,然后测定其质荷比.某有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )
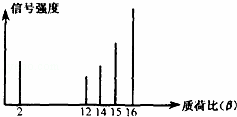
A. 甲醇 B. 甲烷 C. 丙烷 D. 乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com