
【题目】常温下,向100mL0.1mol/LNH4Cl溶液中,逐滴滴加0.1mol/L NaOH溶液。NH4+和NH3·H2O的变化趋势如图所示(不考虑NH3的逸出)。下列说法正确的是

A. M点溶液中水的电离程度比原溶液大
B. 在M点时,n(H+)-n(OH-)=(0.005-a)mol
C. 随着NaOH溶液的滴加,![]() 不断增大
不断增大
D. 当n(NaOH)=0.01mol时,c(NH3·H2O)>c(Na+)>c(OH-)
【答案】B
【解析】分析:图像中有三个特殊点,起点为0.1mol/LNH4Cl溶液,M点为n(NH4+)=0.005mol的溶液,终点为加入0.01molNaOH恰好完全反应的溶液。
详解:A. NH4+水解促进水的电离, M点溶液中c(NH4+)减小,对水的电离促进的减小,所以M点溶液中水的电离程度比原溶液小,A错误;B. 在M点时,根据电荷守恒,n(NH4+)+ n(H+)+n(Na+)= n(OH-)+n(Cl-),此时n(NH4+)=0.005mol,n(Cl-)=0.01mol,n(Na+)=amol,所以n(H+)-n(OH-)=(0.005-a)mol,B正确;C. NH4++H2O![]() NH3
NH3![]() H2O+H+,Kh=
H2O+H+,Kh=![]() ,随着NaOH溶液的滴加,c(NH3
,随着NaOH溶液的滴加,c(NH3![]() H2O)不断增大,所以
H2O)不断增大,所以![]() 不断减小,C错误;D. 当n(NaOH)=0.01mol时,NH4Cl和NaOH恰好完全反应,溶液为等浓度的NaCl和NH3
不断减小,C错误;D. 当n(NaOH)=0.01mol时,NH4Cl和NaOH恰好完全反应,溶液为等浓度的NaCl和NH3![]() H2O 的混合溶液,由于NH3
H2O 的混合溶液,由于NH3![]() H2O发生电离,使c(NH3·H2O)<c(Na+),故D错误;综合以上分析,本题答案为:B。
H2O发生电离,使c(NH3·H2O)<c(Na+),故D错误;综合以上分析,本题答案为:B。


科目:高中化学 来源: 题型:
【题目】某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物![]() 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是
A. 溶液A和B均可以是盐酸或氢氧化钠溶液
B. 溶液A和B均可以选用稀硝酸
C. 若溶液B选用氯化铁溶液,则实验难以实现
D. 实验方案Ⅱ更便于实施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:
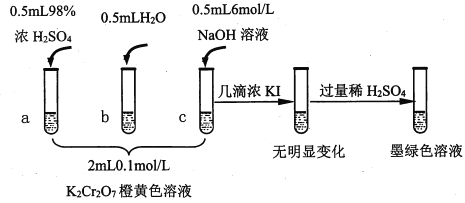
已知:Cr2O72- (橙色)+H2O![]() 2CrO42-(黄色)+2H+ △H= +13.8 kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
2CrO42-(黄色)+2H+ △H= +13.8 kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是________。
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?____(“是”或“否”),理由是_________________________________。
(3)对比试管a、b、c的实验现象,得到的结论是________________。
(4)试管c继续滴加KI溶液、过量稀H2SO4,分析上图的实验现象,得出的结论是_______;写出此过程中氧化还原反应的离子方程式________________。
(5)小组同学用电解法处理含Cr2O72-废水,探究不同因素对含Cr2O72-废水处理的影响,结果如下表所示(Cr2O72-的起始浓度,体积、电压、电解时间均相同)。
实验 | ⅰ | ⅱ | ⅲ | ⅳ |
是否加入Fe2(SO4)3 | 否 | 否 | 加入5g | 否 |
是否加入H2SO4 | 否 | 加入1mL | 加入1mL | 加入1mL |
电极材料 | 阴、阳极均为石墨 | 阴、阳极均为石墨 | 阴、阳极均为石墨 | 阴极为石墨,阳极为铁 |
Cr2O72-的去除率/% | 0.922 | 12.7 | 20.8 | 57.3 |
①实验ⅱ中Cr2O72-放电的电极反应式是________________。
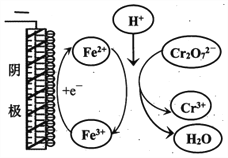
②实验ⅲ中Fe3+去除Cr2O72-的机理如图所示,结合此机理,解释实验iv中Cr2O72-去除率提高较多的原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F( )为一种高分子树脂,其合成路线如下:
)为一种高分子树脂,其合成路线如下:

已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②
请回答下列问题:
(1)X的化学名称是_________________。
(2)E生成F的反应类型为_________________。
(3)D的结构简式为_________________。
(4)由B生成C的化学方程式为_________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和Na2CO3溶液反应放出气体,分子中只有1个侧链,核磁共振氢普显示有5种不同化学环境的氢,峰值面积比为6:2:2:1:1。写出两种符合要求的Y的结构简式___________、__________。
(6)写出以甲醛、丙醛和乙二醇为主要原料合成软质隐形眼镜高分子材料—聚甲基丙烯酸羟乙酯( )的合成路线(无机试剂自选):_________________。
)的合成路线(无机试剂自选):_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制100 mL 1.0 mol/LNa2CO3溶液,下列操作正确的是
A. 称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B. 称取10.6 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解
C. 转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D. 定容后,塞好瓶塞,反复倒转、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
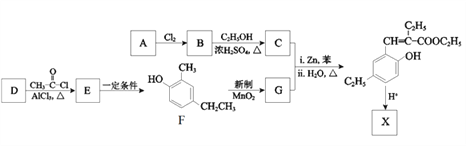
【题目】香豆素类化合物具有芳香气味,是生药中的一类重要的活性成分,主要分布在伞形科、豆科、菊科、芸香科、茄科、瑞香科、兰科等植物中。化合物X是一种香豆素衍生物,可以用作香料,其合成路线如下:
已知: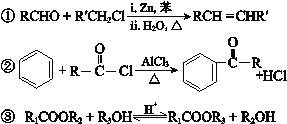
(1)已知A的分子式为C4H8O2。A所含官能团的名称是______________。
(2)B生成C反应的化学方程式是______________________________________________。
(3)G的结构简式是__________________________。
(4)D的分子式是C7H8O,与F互为同系物。则D的结构简式是___________________。
(5)E可以经多步反应合成F,请写出一条可能的合成路线_________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
(6)X的分子式是C13H14O2,X与足量NaOH溶液共热的化学方程式是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨作电极电解下列溶液一段时间后,溶液的pH均增大,再加入一定量括号内的物质,都能使溶液恢复到原来的成分和浓度的是( )
A.AgNO3(AgNO3)B.NaOH (H2O)
C.KCl (KCl)D.CuSO4(CuSO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的现象描述与离子方程式都正确的是
A. 锌片插入硝酸银溶液中,有银析出: ![]()
B. 氢氧化钡溶液与稀硫酸反应,有白色沉淀生成: ![]()
C. 氢氧化铜加到盐酸中, 无明显现象: ![]()
D. 碳酸钡中加入稀盐酸,固体溶解,生成无色无味气体: ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com