
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 常温常压下,4.4g乙醛所含σ键数目为0.7 NA | |
| C. | 标准状况下,5.6L CO2与足量Na2O2反应转移的电子数为0.5 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3 NA |
分析 A.H218O与D2O的摩尔质量都是20g/mol,二者分子中都含有10个中子;
B.根据n=$\frac{m}{M}$计算出4.4g乙醛的物质的量,然后根据乙醛分子中含有6个σ键计算;
C.根据n=$\frac{V}{{V}_{m}}$计算出二氧化碳的物质的量,然后计算出生成氧气的物质的量,根据过氧化钠中氧元素的化合价为-1价计算出转移电子的物质的量及数目;
D.二氧化锰足量,浓盐酸变成稀盐酸后反应停止,则反应生成氯气的物质的量减小,转移电子数减小.
解答 解:A.2.0gH218O与D2O的物质的量为:$\frac{2.0g}{20g/mol}$=0.1mol,二者分子中都含有10个中子,则0.1mol混合物中含有1mol中子,所含中子数为NA,故A正确;
B.4.4g乙醛的物质的量为:$\frac{4.4g}{44g/mol}$=0.1mol,0.1mol乙醛分子中含有σ键的物质的量为:0.1mol×6=0.6mol,其数目为0.6NA,故B错误;
C.标准状况下5.6L二氧化碳的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,0.25mol二氧化碳与足量过氧化钠反应生成0.125mol氧气,转移电子的物质的量为:0.125mol×2=0.25mol,转移的电子数为0.25NA,故C错误;
D.二氧化锰只能与浓盐酸反应,当浓盐酸变成稀盐酸时反应停止,4molHCl反应时转移2mol电子,50mL12mol/L盐酸的物质的量为:n(HCl)=cV=12mol/L×0.05L=0.6mol,0.6mol盐酸不能完全反应,则转移的电子的物质的量小于0.3mol电子,即小于0.3NA个,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;试题有利于培养学生的逻辑推理能力,提高学生的灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2C2O4 | H2S |
| 电离平衡常数 | 1.8×10-5 | Ka1=5.4×10-2 Ka2=5.4×10-5 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
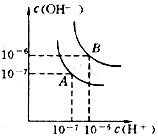 水的电离平衡线如图所示.若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点
水的电离平衡线如图所示.若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中硫酸做还原剂,有铜被还原 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 2mol NH4CuSO3完全反应转移6.02×1023个电子 | |
| D. | 刺激性气味的气体是氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{{r}_{N{a}^{+}}}^{\;}}{{r}_{Na}}$ | B. | $\frac{{r}_{Mg}}{{r}_{Na}}$ | C. | $\frac{{r}_{p}}{{r}_{Cl}}$ | D. | $\frac{{r}_{N}}{{r}_{p}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com