
分析 (1)甲分子中没有支链,能与NaHCO3溶液反应,说明甲分子中含有羧基,结合其分子式写出其结构简式;
(2)乙可发生银镜反应,分子中含有醛基,还能与钠反应,说明分子中含有羟基,据此写出其结构简式;
(3)1mol丙与足量的金属钠反应能生成1molH2,说明丙分子中含有两个羟基;丙还能使溴水褪色,其分子中含有碳碳双键;
(4)丁是一种有果香味的物质,能水解生成A、B两种有机物,则丁为酯类物质;A在一定条件下能转化为B,则丁为乙酸乙酯.
解答 解:(1)甲的分子式为C4H8O2,能够与碳酸氢钠溶液反应,说明含有羧基,且没有支链,则其结构简式为:CH3CH2CH2COOH,
故答案为:CH3CH2CH2COOH;
(2)乙可发生银镜反应,还能与钠反应,说明乙分子中含有醛基和羟基,其可能结构简式如:HOCH2CH2CH2CHO、CH3CH(HO)CH2CHO等,
故答案为:HOCH2CH2CH2CHO;
(3)1mol丙与足量的金属钠反应能生成1molH2,则说明丙分子中含有两个羟基;丙还能使溴水褪色,其分子中含有碳碳双键,结合题中信息可知丙的结构简式可能为:HOCH2CH═CHCH2OH、CH2═CHCH2OHCH2OH等,
故答案为:HOCH2CH═CHCH2OH;
(4)丁是一种有果香味的物质,能水解生成A、B两种有机物,则丁为酯类物质;A在一定条件下能转化为B,则A为乙醇、B为乙酸,故丁为乙酸乙酯,其结构简式为:CH3COOCH2CH3,
故答案为:CH3COOCH2CH3.
点评 本题考查了有机物结构简式的确定、有机物结构与性质,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握同分异构体的概念及书写原则,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| X | Y | ||
| Z | W | M |
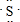 ;它的气态氢化物的结构式为H-S-H.
;它的气态氢化物的结构式为H-S-H.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天然蛋白质水解的最终产物只有一种α氨基酸 | |
| B. | 甘油常应用于化妆品的生产,是因为其具有吸水性 | |
| C. | 淀粉、纤维素、油脂都是高分子化合物 | |
| D. | 苯酚和甲醛都有毒,故不能直接或间接用于制备消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应①是加成反应 | B. | 反应②是加聚反应 | ||
| C. | 反应③是还原反应 | D. | 反应④⑤⑥⑦是取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素和非金属元素间形成的化学键一定是离子键 | |
| B. | 伴有能量变化的物质变化不一定是化学变化 | |
| C. | 可逆反应达到化学平衡时,正逆反应速率都为0 | |
| D. | 通过化学变化可以实现1H与2H间的相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学实验有助于理解化学知识,提升科学素养.某学习小组在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关探究.
化学实验有助于理解化学知识,提升科学素养.某学习小组在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关探究.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com