
| A.用NaHCO3鉴别低级醇和低级羧酸 |
| B.用石墨做电极电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱 |
| C.将氯化铁固体溶解在少量浓盐酸中,然后稀释得到氯化铁溶液 |
| D.淀粉作指示剂,用已知浓度的碘水滴定未知浓度的FeCl2溶液测定其物质的量浓度 |
科目:高中化学 来源:不详 题型:实验题
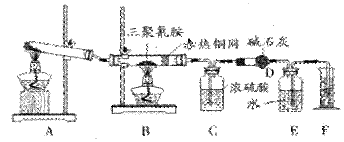

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
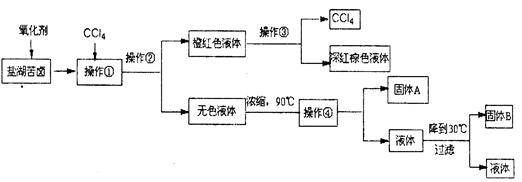
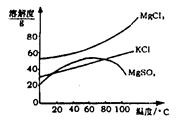
| 化学式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |
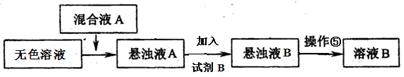
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
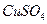 溶液;
溶液;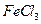 饱和溶液,可以制得
饱和溶液,可以制得 胶体;
胶体; 步骤3加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
步骤3加CCl4,滴加少量氯水,振荡后,CCl4层未变色;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

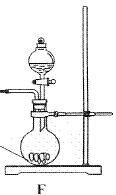
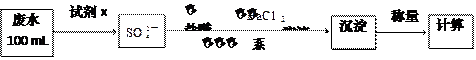
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
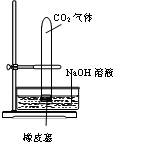 (B)
(B)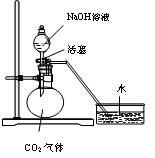
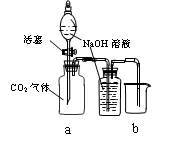 (D)
(D)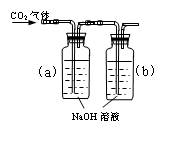
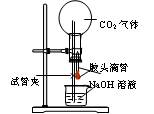
| 装置 | 实验方法 | 实验现象 |
| | | |
| | | |
| | | |
| | | |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
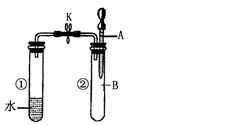
| A.水与氮气 |
| B.稀硫酸与一氧化碳 |
| C.饱和食盐水与氯气 |
| D.浓氢氧化钠溶液与二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com