
下列离子方程式的书写正确的是( )
A.水玻璃中通入过量二氧化硫:Na2SiO3+SO2+H2O═2Na++SO32-+H2SiO3↓
B.铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
C.往碳酸钙中滴加稀盐酸:CO32-+2H+=H2O+CO2↑
D.在NaOH溶液中加入少量Ca(HCO3)2溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
科目:高中化学 来源:2016-2017学年青海省高一上月考一化学试卷(解析版) 题型:填空题
实验室中固体药品应放在 瓶中,取用时块状固体用 取,粉末状固体用 取。液体药品应放在 瓶中,对于见光容易分解的溶液应放在 色的瓶中。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一上月考一化学卷(解析版) 题型:选择题
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数目之比为1∶1
②它们所含的O原子数目之比为1∶2
③它们所含的原子总数目之比为2∶3
④它们所含的C原子数目之比为1∶1
⑤它们所含的电子数目之比为7∶11
A.①和④ B.②和③ C.④和⑤ D.①②③④⑤S
查看答案和解析>>
科目:高中化学 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:填空题
(本题12分)
Ⅰ.某厂废水中含KCN,其浓度为0.01mol·L-1,现用氯氧化法处理,发生如下反应(化合物 中N化合价均为-3价):
中N化合价均为-3价):
(1)KCN+2KOH+Cl2=KOCN+2KCl+H2O被氧化的元素是______________。(用元素符号表示)
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:

(3)若将10 L含KCN的浓度为0.01mol· L-1的废水中KCN氧化除去,最少需要氯气_______mol。
Ⅱ.某实验小组为了测定(3)中溶液多余Cl2的含量,常用Na2S2O3标准溶液进行定量测定。
(4)现实验室需用480mL一定浓度的Na2S2O3溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需 。
(5)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42﹣,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为 。
(6)现取(3)中溶液20.00mL,用a mol·L-1 Na2S2O3溶液进行滴定,经过平行实验测得消耗Na2S2O3标准溶液b mL,计算废液中Cl2的浓度为 mol·L-1 (用含a 、b的表达式表示) 。
查看答案和解析>>
科目:高中化学 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示.下列说法错误的是( )

A.产品FeCO3在空气中高温分解可得到纯净的FeO
B.可利用KSCN溶液检验FeSO4溶液是否变质
C. 沉淀过程中有CO2气体放出
沉淀过程中有CO2气体放出
D.检验沉淀是否洗涤干净可用盐酸酸化的BaCl2溶液
查看答案和解析>>
科目:高中化学 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
区别硝石(KNO3)和朴消(Na2SO4):“以火烧之,紫青烟起,乃真硝石也”--《本草经集注》,这里运用了硝石的哪些性质:
A.焰色反应 B.氧化性 C.还原性 D.不稳定性
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:选择题
分别依据下列实验事实,得出的结论正确的是
实验事实 | 结论 | |
A | 苯酚和水的浊液中,加碳酸钠溶液,溶液变澄清 | 苯酚的酸性比碳酸强 |
B | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 | 随溶液pH减小,“84”消毒液的氧化能力增强 |
C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
D | 向2 mL 0.1 mol/L的硝酸银溶液中加入1 mL0.1 mol/L NaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L Na2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市高一10月月考化学卷(解析版) 题型:实验题
I、如图为实验室蒸馏自来水得到少量蒸馏水的装置示意图,请根据图示回答下列问题:
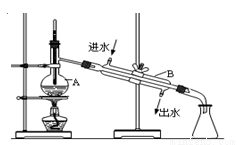
(1)装置中仪器A的名称是 。
(2)请指出上图中的两处明显错误: 、 。
(3)实 验时A中除加入少量自来水外,还需加入少量的沸石,其作用是 。
验时A中除加入少量自来水外,还需加入少量的沸石,其作用是 。
II、选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B升华 C结晶 D分液 E蒸馏 F过滤
(1) 分离饱和食盐水与沙子的混合物;
(2) 从硝酸钾和氯化钠的混合液中获得硝酸钾;
(3) 分离水和汽油的混合物;
(4) 分离 CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二10月月考化学卷(解析版) 题型:选择题
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积(容器容积)的关系如下表所示:
nY(g) ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积(容器容积)的关系如下表所示:
气体体积/L c (Y)/mol·L-1 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1. | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com