
某兴趣小组用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入右图装置(电极均为惰性材料)进行实验。下列说法正确的是

A. N极为负极
B. 反应一段时间后,左侧电解质溶液的pH增大
C. M极发生的电极反应为SO2+2H2O-2e-=SO42-+4H+
D. 在相同条件下,M、N两极上消耗的气体体积之比为1:2
科目:高中化学 来源:2016-2017学年浙江省台州市高二上学期期末质量评估考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 含H+的溶液显酸性 B. 加热蒸馏水,Kw变大,pH变小
C. 常温下,0.01mol·L-1的Ba(OH)2溶液pH为12 D. 醋酸溶液加水稀释,所有离子的浓度都减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宿州市高一上学期期末教学质量检测(a卷)化学试卷(解析版) 题型:选择题
向MgC12和AlC13的混合溶液中,逐滴滴加1mol/L的氨水至过量,下列关系图中最合理的是
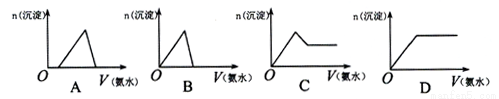
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:实验题
[实验化学]
实验室以苯甲酸和乙醇为原料制备甲酸乙酯(实验装置如图所示,相关物质的沸点如下表)。其实验步骤如下:
物质 | 苯甲酸 | 乙醇 | 环己烷 | 浓硫酸 | 苯甲酸乙酯 |
沸点/℃ | 249 | 78.3 | 80.7 | 338 | 212.6 |
步骤1:将三颈瓶中的苯甲酸、乙醇、浓硫酸和环己烷按一定配比充分混合后,升温至60 ℃。
步骤2:将反应混合物倒入分液漏斗中,静置、分液。
步骤3:向上层液体中加入乙醚,再向混合液中加入饱和碳酸钠溶液,分离出乙醚层。
步骤4:向乙醚层中加入固体氯化钙后进行蒸馏,收集相应馏分。
(1)反应容器中制取苯甲酸乙酯的化学方程式为_____;实验装置中冷凝管的主要作用是_________。
(2)向反应体系中加入环己烷,可以提高产物效率的原因是_______________。
(3)步骤4中加入固体氯化钙的作用是___________。
(4)向反应体系中加入苯也可以制取苯甲酸乙酯,用环己烷代替苯的优点是____________。
(5)步骤3中加入乙醚和饱和碳酸钠溶液的作用是__________。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
一定条件下,在三个容积均为2L的恒容密闭容器中发生反应:H2(g)+CO2(g)  HCOOH(g)。下列说法正确的是
HCOOH(g)。下列说法正确的是
容器编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/mol | |
H2 | CO2 | HCOOH | |||
Ⅰ | 150 | 0.4 | 0.4 | 0.2 | 2 |
Ⅱ | 150 | 0.8 | 0.8 | t1 | |
Ⅲ | 0.4 | 0.4 | 0.16 | t2 | |
A. 反应达到平衡时,容器Ⅰ中的平均反应速率为v(H2)=0.1mol/(L·min)
B. 反应达到平衡时,容器Ⅱ所需时间t2<2min
C. 若只改变一个反应条件,容器Ⅲ可能是加入了合适的催化剂
D. 起始时,向容器Ⅱ中充入0.45mol H2、0.20mol CO2 和0.18molHCOOH,则反应向正反应方向进行
查看答案和解析>>
科目:高中化学 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A. 用醋酸除去水垢中的碳酸钙:CaCO3+2H+ =Ca2++H2O+CO2↑
B. 硫化钠水溶液呈碱性的原因:S2-+2H2O H2S↑+2OH-
H2S↑+2OH-
C. 向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++OH- +HCO3- = BaCO3↓+ 2H2O
D. 向Na2FeO4溶液中加入稀硫酸产生氧气: 4FeO42-+20H+=4Fe3++3O2↑+10H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一下学期期初化学试卷(解析版) 题型:简答题
Ⅰ. 有一瓶澄清溶液,可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl―、I―现进行如下实验:
①测知溶液显强酸性;②取样加少量CCl4和数滴新制氯水,CCl4层为紫红色;
③另取样滴加稀NaOH溶液,使溶液变为碱性,此过程中均无沉淀生成;
④取少量上述碱性溶液,加Na2CO3溶液出现白色沉淀;
⑤将实验③中的碱性溶液加热,有气体放出,该气体能使湿红色石蕊试纸变蓝。
请回答:(1)原溶液中肯定存在的离子是____________________
(2)不能确定是否存在的离子是____________________
Ⅱ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: NO3-+ 4H++3e-→NO↑+ 2H2O
其中KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式______________________________。
(2)反应中硝酸体现了________________、_______________性质。
(3)反应中若产生0.2mol气体,则转移电子的数目是_____________。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是_______
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一下学期期初化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A. 钠与水反应:Na+H2O= Na++OH-+H2↑
B. 铁与硫酸铁溶液反应:Fe+Fe3+ = 2Fe2+
C. 氢氧化镁与稀盐酸反应:Mg(OH)2+2 H+ = Mg2++2H2O
D. 碳酸氢钠溶液中滴入氢氧化钠溶液:OH —+HCO3-= H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:河北省2016-2017学年高一下学期开学考试化学试卷 题型:选择题
向Fe 2 (SO 4 ) 3 和Al 2 (SO 4 ) 3 的混合溶液中,逐滴加入NaOH溶液至过量。下列图象中,能正确表示上述反应的是
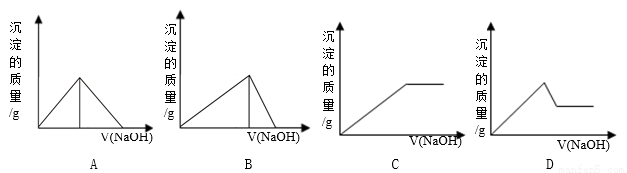
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com