
【题目】下列说法中正确的是( )
A.铅蓄电池放电时,负极质量减轻,正极增重
B.升高CH3COONa溶液的温度,其水的离子积常数和pH均增大
C.CH3CH=CHCH3分子中的四个碳原子都在一条直线上
D.常温下Ksp(AgBr)=5.0×10-13,Ksp(AgCl)=1.8×10-10,则S(AgBr)>S(AgCl)
【答案】B
【解析】
A.铅蓄电池的负极反应为Pb-2e-+SO42-=PbSO4,负极由Pb转化为PbSO4,质量增加;正极反应为PbO2+2e-+SO42-+4H+=PbSO4+2H2O,由PbO2转化为PbSO4,质量增加,A错误;
B.CH3COONa溶液中存在CH3COO-水解,CH3COO-+H2O![]() CH3COOH+OH-,也有水的电离,H2O
CH3COOH+OH-,也有水的电离,H2O![]() H++OH-。升高温度,水的电离被促进,水的离子积常数增大;CH3COO-的水解被促进,c(OH-)增大,pH增大,B正确;
H++OH-。升高温度,水的电离被促进,水的离子积常数增大;CH3COO-的水解被促进,c(OH-)增大,pH增大,B正确;
C.碳碳双键的碳原子与和其连接的原子形成的键角约为120°,因此CH3CH=CHCH3中的4个C原子没有在一条直线上,C错误;
D.对于同一类型的难溶物,可以根据它们Ksp的大小,比较它们溶解度的大小。Ksp(AgBr)<Ksp(AgCl),则S(AgBr)<S(AgCl),D错误。
答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A.用 Na2CO3 溶液将水垢中的 CaSO4 转化为 CaCO3:CO3 2-+Ca2+ =CaCO3↓
B.电解饱和食盐水产生黄绿色气体:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
C.红热木炭遇浓硝酸产生红棕色气体:C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
D.用新制 Cu(OH)2 检验乙醛,产生红色沉淀:CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O
CH3COONa+Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中发生反应:![]() 。下列叙述中不能说明上述反应已达到化学平衡状态的是
。下列叙述中不能说明上述反应已达到化学平衡状态的是
A.混合气体的密度不变
B.体系的压强不变
C.混合气体的平均相对分子质量不变
D.反应体系中乙醇的物质的量浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
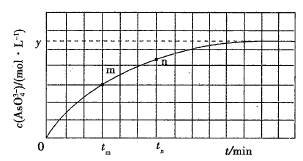
下列可判断反应达到平衡的是__(填标号)
a溶液的pH不再变化
b.v(I-)=2v(AsO33-)
c.![]() 不再变化
不再变化
d.c(I-)=ymol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4(阱)可作制药的原料,也可作火箭的燃料。已知热化学方程式:
反应I:N2H4(g)![]() N2(g)+2H2(g) △H1>0;
N2(g)+2H2(g) △H1>0;
反应II:N2(g)+3H2(g)![]() 2NH3(g) △H2<0;
2NH3(g) △H2<0;
反应III:N2H4(g)+H2(g)![]() 2NH3(g) △H。
2NH3(g) △H。
下列推断不正确的是( )
A.N2H4断裂共价键需要吸收能量
B.反应I中1molN2H4(g)的能量小于1molN2(g)和2molH2(g)的总能量
C.反应II中正反应的活化能大于逆反应的活化能
D.△H=△H1+△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥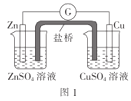
B.图2:可根据该实验验证铁的吸氧腐蚀
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应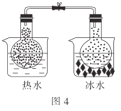
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
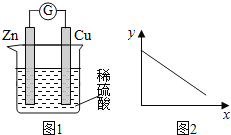
A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,分别在下列容积为2L的恒容绝热密闭容器中,发生如下反应: 2CO(g)+SO2(g)=S(g)+2CO2(g) △H>0。测得相关数据如下表所示。
容器 | 起始时物质的量 | 平衡时CO(g)的浓度/mol·L | |||
CO(g) | SO2(g) | S(g) | CO2(g) | ||
甲 | 1 | 0.5 | 0.5 | 1 | a |
乙 | 1 | 0.5 | 0 | 0 | 0.2 |
丙 | 0 | 0 | 1 | 2 | b |
下列说法正确的是
A.平衡常数:K甲>K乙
B.a=0.4
C.若乙容器l0min达到平衡.则用S(g)表示的反应速率为0.005molL-1min-1
D.若将丙容器改为恒压绝热容器,则达到平衡时b=0.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)在工业生产中应用广泛。它在催化剂作用下与水反应获取氢气的微观过程如图所示。下列说法正确的是( )
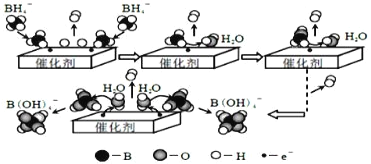
A.水在此过程中作还原剂
B.若将NaBH4中的H用D代替,反应后生成的气体中含有H2、HD和D2
C.催化剂可以加快反应速率,其用量多少不影响反应速率
D.NaBH4与水反应的离子方程式为:BH4-+4H2O=B(OH)4-+4H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com