
��7�֣��ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϣ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
��CH4��g��+H2O��g��⇌CO��g��+3H2��g����H1=+206��1kJ/mol
��CH4��g��+CO2��g��⇌2CO��g��+2H2��g����H2=+247��3kJ/mol
��CO��g��+H2O��g��⇌CO2��g��+H2��g����H3

��ش��������⣺
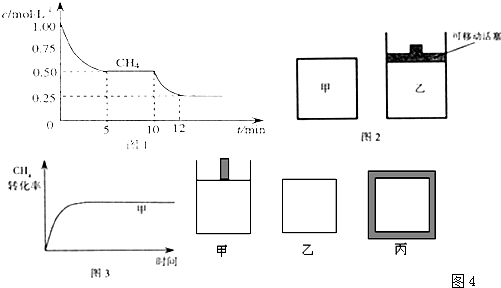
��1����һ�����ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5min�ڣ���H2��= ��10minʱ���ı��������������� ��
��2����ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȣ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䣮��֪��������CH4��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������CH4��ת������ʱ��仯��ͼ��
��3����Ӧ���С�H3= ��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K=1��0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±���
|
CO |
H2O |
CO2 |
H2 |
|
0��5mol |
8��5mol |
2��0mol |
2��0mol |
��ʱ��Ӧ���������淴Ӧ���ʵĹ�ϵʽ�� ������ţ���
a��v��������v���棩 b��v��������v���棩
c��v������=v���棩 d�����жϣ�
��1�� 0��3mol/��L•min�� �����¶�
��2�� ��
��
��3����41��2kJ/mol a
��������
�����������1����ͼ1��֪��ǰ5min�ڼ����Ũ�ȱ仯Ϊ0��50 mol��L��1������v=��c/��t����v(CH4)= 0��1mol/��L•min����Ϸ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȼ���ɵ�v(H2)= 0��3mol/��L•min����ע��д�嵥λ����ͼ1��֪��10minʱ�����Ũ�ȼ�����С���÷�Ӧ������Ӧ�����ƶ������÷�ӦΪ���ȷ�Ӧ����ı����������Ϊ�����¶ȡ���2����ͼ1�������֪�������ķ�Ӧ����Ϊ���µ��ݣ��������ķ�Ӧ����Ϊ���µ�ѹ���ס����������зֱ��������ʵ�����CH4��CO2���Ҽס�����������ʼ�ݻ���ȣ���������䣬�ҵ�ѹǿ���䣬��ٶ��ײ��䣬���з���CH4��g��+CO2��g��⇌2CO��g��+2H2��g����������������൱��ѹǿ��С����ѧƽ��������Ӧ�����ƶ�����������CH4��ת��������ѹǿС����Ӧ���ʼ�������ﵽƽ���ʱ��䳤���ɴ˿ɻ���ͼ��3�����ݸ�˹���ɿ�֪����-�ڿɵ÷�Ӧ�ۣ����H3=+206��1kJ/mol-��+247��3kJ/mol��=-41��2kJ/mol��800��ʱ����Ӧ�۵�K=1��0ʱ������������ͬһ�ܱ������У������ͬ�������ʵ�����Ũ�ȳ����ȣ��ɱ����е����ݼ����Q��K���÷�Ӧ������Ӧ�����ƶ���������Ӧ���ʴ����淴Ӧ���ʣ���ѡa��
���㣺���黯ѧ��Ӧ���ʵļ��㣬��ѧƽ����ƶ�����Ӧ������жϡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�



| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϡ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
�� CH4(g)��H2O(g)![]() CO(g)��3H2(g) ��H1����206.1 kJ/mol
CO(g)��3H2(g) ��H1����206.1 kJ/mol
�� CH4(g)��CO2(g)![]() 2CO(g)��2H2(g) ��H2����247.3 kJ/mol
2CO(g)��2H2(g) ��H2����247.3 kJ/mol
�� CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H3
CO2(g)��H2(g) ��H3
��ش��������⣺
�� ��һ�ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5 min�ڣ� v(H2)�� �� ��10 minʱ���ı��������������� �� ��
![]()

�� ��ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������CH4��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������CH4��ת������ʱ��仯��ͼ��

�� ��Ӧ���Ц�H3�� �� ��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K��1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±���
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
��ʱ��Ӧ���������淴Ӧ���ʵĹ�ϵʽ�� �� ������ţ���
a��v(��)��v(��) b��v(��)��v(��) c��v(��)��v(��) d�����ж�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com