
| A. | 转移时,要用玻璃棒引流 | |
| B. | 托盘天平称取58.50克食盐,加水配制成1升溶液,NaCl溶液浓度为1mol•L-1 | |
| C. | 溶解食盐的烧杯要洗涤2~3次并将洗涤液转移到容量瓶中 | |
| D. | 搅拌可加速溶解 |
分析 A.容量瓶瓶口较细,移液时应用玻璃棒引流,防止液体洒在容量瓶外边;
B.托盘天平精确度为0.1g;
C.为防止配制溶液的浓度偏小,洗涤液也要转移到容量瓶中;
D.搅拌可加速溶解.
解答 解:A.转移时,要用玻璃棒引流,防止液体洒在容量瓶外边,导致配制溶液浓度不准确,故A正确;
B.托盘天平称取58.5g食盐,加水配制成1升溶液,NaCl溶液浓度为1mol•L-1,故B错误;
C.溶解食盐的烧瓶沾有溶质,如果不将洗涤液转移到容量瓶中会导致配制溶液的物质的量浓度偏低,所以溶解食盐的烧杯要洗涤2~3次并将洗涤液转移到容量瓶中,故C正确;
D.搅拌可加速溶解,故D正确;
故选:B.
点评 本题考查了一定物质的量浓度溶液的配制,熟悉相关实验的基本操作是解题关键,注意托盘天平的使用方法和精确度,注意玻璃棒在配制溶液过程中的作用.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V=2.24L | |
| B. | 参加反应的HCl为0.18mol | |
| C. | 无法确定最终生成含钾化合物的数量是多少 | |
| D. | 6.32g KMnO4粉末若直接与足量浓盐酸反应可得到2.24L Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ;某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):回答下列问题:
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ;某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
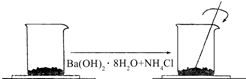 在一个小烧杯里,加入 40g Ba(OH)2•8H2O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上.然后加入20g NH4Cl晶体,并用玻璃棒迅速搅拌.如图所示.回答下列问题:
在一个小烧杯里,加入 40g Ba(OH)2•8H2O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上.然后加入20g NH4Cl晶体,并用玻璃棒迅速搅拌.如图所示.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com