
下列事实不能用平衡移动原理解释的是( )
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.工业合成氨时采用铁触媒作反应的催化剂
C.工业生产硫酸的过程中使用过量的空气以提高SO2的转化率
D.将收集NO2气体的烧瓶密闭后放在装有热水的烧杯中,发生颜色变化
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源:2017届山东省栖霞市高三上学期期中化学试卷(解析版) 题型:实验题
化学小组设计以下实验方案,测定某部分变质为碳酸钠的小苏打样品中NaHCO3的质量分数。
(1)方案一:称取一定质量样品,置于仪器a中用酒精灯加热至恒重,冷却,用托盘天平称量剩余固体质量。重复操作,计算。
仪器a的名称是____________;其中发生反应的化学方程式为_______________。实验中为保证NaHCO3分解完全需加热至恒重,判断方法是________________。
⑵方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,待沉淀后,过滤,洗涤,干燥,称量固体质量,计算。
写出NaHCO3与足量Ba(OH)2溶液反应的离子方程式_______________;实验中判断沉淀是否完全的方法是______________。过滤操作中,除烧杯、漏斗外,还要用到的玻璃仪器为____________。
(3)方案三:称取一定质量样品,按如图装置进行实验:
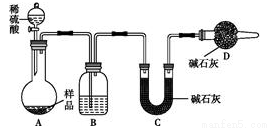
B装置内所盛试剂是;D装置的作用是______________。实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为________。某同学认为上述测定结果__________(填“偏高”或“偏低”),因为实验装置还存在一个明显的缺陷是 。
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月月考化学试卷(解析版) 题型:实验题
工业上利用含镍废料(镍铁钙镁合金为主)制取草酸镍(NiC2O4﹒H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐难溶于水。根据下列工艺流程示意图回答问题。
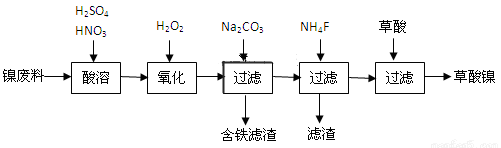
(1)Fe在元素周期表中的位置 _______________________________
(2)生产过程中多次进行过滤,玻璃棒在过滤操作中的一个作用是引流,下列实验操作中玻璃棒起引流作用的是 (填选项字母)
A.测定Na2CO3溶液的PH 
B.配制0.1mol/L 的H2SO4溶液
C.加热NaCl溶液制备NaCl晶体
D.验证Ba(OH)2 · 8H2O与NH4Cl固体反应吸热
(3)①加入H2O2发生的主要反应的离子方程式为_______________________
②加入NH4F后除掉的杂质是_____________________
(4)草酸镍(NiC2O4·2H2O)在热空气中干燥脱水后在高温下煅烧三小时,制得三氧化二镍,同时获得混合气体。无水草酸镍受热分解的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:填空题
氨对地球上的生物相当重要,它是许多食物和肥料的重要成分。氨也是制造硝酸、化肥、炸药 的重要原料。氨在国民经济中占有重要地位。回答下列问题:
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
①工业合成氨的热化学方程式是_______________。
②若起始时向容器内放入1 mol N2和3 mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为____________;若在同体积的容器中充人2 mol N2和6 molH2,达平衡后放出的热量为Q2 kJ,则Q2__________(填“>”、“<”或“=”)2Q1。
③已知:

1 mol N-H键断裂吸收的能量约等于__________kJ。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2 (g)+3H2 (g) 2NH3 (g),其平衡常数K与温度T的关系如下表:
2NH3 (g),其平衡常数K与温度T的关系如下表:

①平衡常数表达式K=_________,K1___________(填“>”、“<”或“一”)K2。
②一定温度下,下列各项能作为判断该反应达到化学平衡状态的依据是__________(填字母)。
a.容器内N2、H2、NH3的浓度之比为1: 3:2
b.浓度商Q=平衡常数K
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2 mol、1 mol、2 mol时,则此时该反应_________(填“处于”或“不处于”)平衡状态。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:选择题
已知:H2(g)+1/2O2(g)=H2O(g) △H=akJ·mol-l
2H2(g)+O2(g)=2H2O(g) △H=bkJ·mol-l
H2(g)+1/2O2(g)=H2O(1) △H=ckJ·mol-l
2H2(g)+O2(g)=2H2O(1) △H=dkJ·mol-l
下列关系式中正确的是
A. a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:选择题
金属锡的冶炼常用焦炭作还原剂:SnO2+2C=Sn+2CO↑,反应过程中能量的变化如图所示。下列有关该反应的△H、△S的说法中正确的是( )
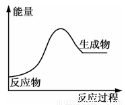
A.△H<0,△S<0 B.△H>0,△S<0
C.△H>0,△S>0 D.△H<0,△S>0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:实验题
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
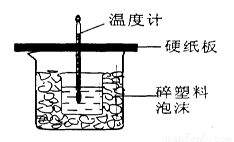
(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_____ _______。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值___________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,
与上述实验相比,所放出的热量____________(填“相等”或“不相等”),所求中和热的数值会____________(填“相等”或“不相等”),理由是_____________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是
A、铜片作原电池的负极,石墨作原电池的正极,氯化钠作电解质溶液
B、铜锌合金在潮湿空气发生电化学腐蚀
C、用铜片作阴、阳电极,电解硫酸钠溶液
D、用铜片作阴、阳电极,电解硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市岐山县高三上期中化学试卷(解析版) 题型:选择题
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是

A. 非金属性:Z<T<X
B. R与Q的电子数相差26
C. 气态氢化物稳定性:R <T<Q
D. 最高价氧化物的水化物的酸性: X > T
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com