
甲醇(CH3OH)是一种优质燃料,(1)已知一定条件下每1molCO2和足量氢气完全反应三可生成1mol气态甲醇(CH3OH)和1mol 水蒸汽并放出49kJ的热量.请回答:
①该反应的热化学方程式: .
②其反应过程中能量的变化与如图1所示最相符的是 .

(2)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应,测得CO2和CH3OH(g)的浓度随时间变化如图2.请回答:
①从反应开始到平衡,甲醇和氢气的反应速率:
v(CH3OH)=
v(H2)= .
②下列措施中能使v (CO2)增大的是 .
A.加入催化剂 B.充入He(g),使体系压强增大C.将H2O(g)从体系中分离 D.升高温度
③能够说明该反应已达到平衡的是 .
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度不再变化
D.一定条件下,单位时间内消耗3molH2的同时生成1molCH3OH.
考点: 热化学方程式;反应速率的定量表示方法;化学平衡的影响因素;化学平衡状态的判断.
分析: (1)①每1molCO2和足量氢气完全反应三可生成1mol气态甲醇(CH3OH)和1mol 水蒸汽并放出49kJ的热量,据此写出热化学方程式;
②由①可知该反应为放热反应,则反应物总能量大于生成物总能量,据此分析;
(2)在体积为l L的密闭容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L;
①依据化学平衡三段式列式利用V= 计算;
计算;
②依据升温,增加浓度,加压,加催化剂等可以加快反应速率判断;
③可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析解答.
解答: 解:(1)①每1molCO2和足量氢气完全反应三可生成1mol气态甲醇(CH3OH)和1mol 水蒸汽并放出49kJ的热量,则热化学方程式为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol,故答案为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol;
②由①可知该反应为放热反应,则反应物总能量大于生成物总能量,所以能量的变化与如图1所示最相符的是A,故选:A;
(2)在体积为l L的密闭容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L;则①依据化学平衡列式计算为:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
起始量(mol/L) 1 3 0 0
变化量(mol/L) 0.75 2.25 0.75 0.75
平衡量(mol/L) 0.25 0.75 0.75 0.75
CH3OH的平均反应速率v(CH3OH)= =0.075mol•L﹣1•min﹣1 ,H2的平均反应速率v(H2)=
=0.075mol•L﹣1•min﹣1 ,H2的平均反应速率v(H2)= =0.225mol•L﹣1•min﹣1 ;
=0.225mol•L﹣1•min﹣1 ;
故答案为:0.075 mol•L﹣1•min﹣1;0.225mol•L﹣1•min﹣1 ;
②A.加入催化剂,v (CO2)增大,故A正确;
B.充入He(g),使体系压强增大,但反应物浓度不变,所以v (CO2)不变,故B错误;
C.将H2O(g)从体系中分离,则生成物浓度减小,则浓度减小,故C错误;
D.升高温度,v (CO2)增大,故D正确;
故选:AD;
③A.反应前后气体的体积不等,所以压强一直在变,则当压强不变时能说明达到平衡,故A正确;
B.反应前后质量不变,体积也不变,所以密度一直不变,则混合气体的密度不再变化不能说明达到平衡,故B错误;
C.CO2、H2和CH3OH的浓度不再变化,说明达到平衡,故C正确;
D.单位时间内消耗3molH2的同时生成1molCH3OH,都是指正反应方向,不能说明达到平衡,故D错误;
故选AC;
点评: 本题考查了热化学方程式的书写原则,化学反应速率、平衡状态的判断以及化学平衡的计算的应用,图象分析是关键,综合性较大,难度中等.


科目:高中化学 来源: 题型:
可逆反应A(g)+B(g)
 2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
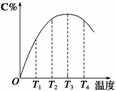
①由T1向T2变化时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
②由T3向T4变化时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
③反应在________温度下达到平衡。
④此反应的正反应为______热反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.合成氨反应中,断开1 mol N≡N键,就会同时生成6 molN—H键,此时达化学平衡状态
B.有气体参与的可逆反应中,当反应容器中的压强保持不变时,即达到化学平衡状态
C.当反应物或生成物在混合物中的百分含量保持不变时,即达到化学平衡状态
D.工业生产中采用高温是因为高温下反应物的转化率比低温时高
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
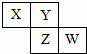
A. Z单质与氢气反应较Y剧烈
B. 最高价氧化物对应水化物酸性W比Z强
C. X单质氧化性强于Y单质
D. X与W的原子核外电子数相差9
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 需要加热的化学反应都是吸热反应
B. 陶瓷、玻璃和水泥都是无机非金属材料
C. 醋酸、蔗糖均属于电解质
D. 糖类、油脂和蛋白质都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知丙烷的二氯代物C3H6Cl2有4种同分异构体,则分子式为C3H2Cl6的同分异构体共有(不考虑立体异构)( )
A. 3种 B. 4种 C. 5种 D. 6种
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2↑
④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑
⑥SiO2+2NaOH=Na2SiO3+H2O
(1)上述反应中不属于氧化还原反应的有 (填序号,下同).H2O被氧化的是 H2O被还原的是 .属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是 .
(2)写出方程式②的离子方程式 .
(3)标出方程式④的电子转移的方向和数目 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com