
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/mn | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 | |
| B. | 元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 | |
| C. | 元素②⑥形成的化合物具有两性 | |
| D. | 元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强 |
分析 ②⑤的最低价都为-2价,应该为ⅥA族元素,原子半径②<⑤,则②为O元素、⑤为S元素;①⑦⑧的最高正化合价为+1价,原子半径①<O<⑦<⑧,则①为H元素、⑦为Li元素、⑧为Na元素;③⑥的最高价为+3价,原子半径③<⑦,则③为B元素、⑥为Al元素;④的最低价为-1价,为ⅤⅡA族元素,其原子半径大于O元素,则④为Cl元素,结合元素周期律知识进行解答.
解答 解:②⑤的最低价都为-2价,应该为ⅥA族元素,原子半径②<⑤,则②为O元素、⑤为S元素;①⑦⑧的最高正化合价为+1价,原子半径①<O<⑦<⑧,则①为H元素、⑦为Li元素、⑧为Na元素;③⑥的最高价为+3价,原子半径③<⑦,则③为B元素、⑥为Al元素;④的最低价为-1价,为ⅤⅡA族元素,其原子半径大于O元素,则④为Cl元素.
A.由于非金属性:Cl>S,则氢化物稳定HCl>H2S,故A正确;
B.元素②气态氢化物为水,元素⑤气态氢化物为硫化氢,由于水分子中存在氢键,则水的沸点大于硫化氢,故B错误;
C.元素②⑥形成的化合物为氧化铝,氧化铝为两性氧化物,故C正确;
D.元素④的最高价氧化物的水化物高氯酸,元素⑤的最高价氧化物的水化物为硫酸,由于非金属性:Cl>S,则高氯酸的酸性大于硫酸,故D正确;
故选B.
点评 本题考查结构性质位置关系应用,关键是根据化合价与原子半径推断元素,注意熟练掌握元素周期表结构、元素周期律的内容,注意氢键对物质性质的影响.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题

| A. | 原子半径由大到小的顺序:X、Y、Z、W | |
| B. | 元素最高正价由低到高的顺序:X、Y、Z、W | |
| C. | 简单氢化物的热稳定性由弱到强的顺序:Y、Z、W | |
| D. | 最高价氧化物的水化物的酸性由弱到强的顺序:X、Y、Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | II A | III A | IV A | VA | VI A | VII A |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
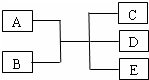 已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.
已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 蒸发结晶时应将溶液蒸干 | |
| D. | 称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称氢氧化钠时,不能直接称量,也不能放在称量纸上 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从下口倒出 | |
| D. | 过滤时,玻璃棒的末端应轻轻靠在三层的滤纸上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H8 | B. | C3H8O2 | C. | C2H6O | D. | C3H6O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com