
对于在一定条件下进行的化学反应:2SO2+O2?2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是( )
A.升高温度 B.增大压强 C.减小反应物浓度 D.增大反应物浓度
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源:2017届广东省肇庆市高三上学期二模化学试卷(解析版) 题型:填空题
为了有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物含量、使用清洁能源显得尤为重要。
(1)已知:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ∆H = -905.48 kJ·mol-1
4NO(g)+6H2O(g) ∆H = -905.48 kJ·mol-1
N2(g)+O2(g) 2NO(g) ∆H = +180.50 kJ·mol-1
2NO(g) ∆H = +180.50 kJ·mol-1
则4NH3(g)+6NO(g) 5N2(g)+6H2O(g)的∆H = 。
5N2(g)+6H2O(g)的∆H = 。
(2)某化学小组查阅资料知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g) N2O2(g) (快) ∆H1<0 v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
N2O2(g) (快) ∆H1<0 v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g) 2NO2(g) (慢) ∆H2< 0
2NO2(g) (慢) ∆H2< 0
v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
① 2NO(g)+O2(g) 2NO2(g)的反应速率主要是由_______(填“第一步”或“第二步”)反应决定。
2NO2(g)的反应速率主要是由_______(填“第一步”或“第二步”)反应决定。
② 一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K= ;升高温度,K值 (填“增大”、“减 小”或“不变”)
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K= ;升高温度,K值 (填“增大”、“减 小”或“不变”)
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g) N2(g)+xCO2(g) △H <0;理论上,适当增加汽车排气管(内壁为活性炭涂层)长度______(填“能”或“不能”)使NOx更加有效地转化为无毒尾气而排放,其原因是 。
N2(g)+xCO2(g) △H <0;理论上,适当增加汽车排气管(内壁为活性炭涂层)长度______(填“能”或“不能”)使NOx更加有效地转化为无毒尾气而排放,其原因是 。
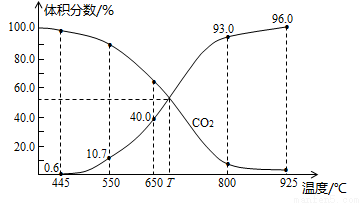
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应: C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示,则800℃时,反应达平衡时CO2的转化率为________(保留一位小数)。
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示,则800℃时,反应达平衡时CO2的转化率为________(保留一位小数)。
(5)氢气是一种重要的清洁能源,Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2017届广东省韶关市高三上高考调研理综化学试卷(解析版) 题型:选择题
化学与社会、科学、技术、环境等有密切联系。下列有关说法正确的是
A.用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的
B.PM 2.5是指氮、硫的氧化物溶于水形成的酸性液体造成的空气污染
C.新型材料聚酯纤维、光导纤维都属于有机高分子
D.在食品袋中放入盛有硅胶的透气袋,可防止食物氧化变质
查看答案和解析>>
科目:高中化学 来源:2017届广东省清远市清城区高三上期末B卷化学试卷(解析版) 题型:选择题
以下自发进行反应可用能量判据来解释的是( )
A.硝酸铵自发地溶于水
B.2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ•mol﹣1
C.(NH4 )2 CO3(s)═NH4HCO3(s)+NH3(g);△H=+74.9 kJ/mol
D.2H2(g)+O2(g)═2H2O(l);△H=﹣571.6 KJ/mol
查看答案和解析>>
科目:高中化学 来源:2017届广东省清远市清城区高三上期末B卷化学试卷(解析版) 题型:选择题
X、Y、Z都是气体,反应前X、Y的物质的量之比是1:2,在一定条件下可逆反应X+2Y?2Z达到平衡时,测得反应物总的物质的量等于生成物总的物质的量,则平衡时X的转化率是( )
A.80% B.20% C.40% D.60%
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三1月诊断性考试化学试卷(解析版) 题型:实验题
电石广泛用于生产PVC、维尼纶等,电石与水反应所得残渣——电石渣,主要含Ca(OH)2、CaCO3及少量其他杂质。某工业电石渣的几种回收利用流程如下:
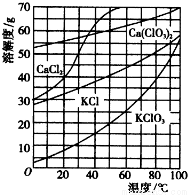
几种物质在水中的溶解度曲线如右图。回答下列问题:
(1)常温氯化
①反应的化学方程式是 。
②提高Cl2转化为Ca(ClO)2的转化率可行的措施有_______(填序号)。
A.加热升高温度 B.适当减缓通入Cl2速率
C.充分搅拌浆料 D.加水使Ca(OH)2完全溶解
③电石渣中的有害杂质CN-与ClO-反应转化为两种无害的气体,每转化1 mol CN-至少需要消耗氧化剂ClO-_______mol。
(2)75 ℃氯化
①生成氯酸钙中氯的化合价为 ,氯化完成后过滤,滤渣的主要成分为______(填化学式)。
②氯酸钙能与KCl反应转化为氯酸钾的原因是 。
(3)有机反应
首先生成氯代乙醇,其结构简式为 ,氯代乙醇再与Ca(OH)2反应生产环氧乙烷。总反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三1月诊断性考试化学试卷(解析版) 题型:选择题
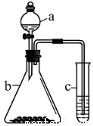
利用右下图所示装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测其中现象正确的是
选项 | a | b | c | c试管中现象 |
A | 浓盐酸 | KMnO4 | FeCl2溶液 | 溶液变棕黄色 |
B | 稀硫酸 | Na2S2O3 | 溴水 | 产生浅黄色沉淀 |
C | 硼酸 | Na2CO3 | Na2SiO3溶液 | 析出白色沉淀 |
D | 浓硝酸 | 铁片 | KI-淀粉溶液 | 溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源:2017届山东省潍坊市临朐县高三12月阶段测化学试卷(解析版) 题型:选择题
下列离子在指定溶液中一定能大量共存的是
A.能使甲基橙变红的溶液中:Fe2+、Al3+、NO 、Cl-
、Cl-
B.在pH=12的溶液中:Na+、AlO 、NO
、NO 、S2-
、S2-
C.室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO 、NO
、NO 、NH
、NH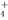
D.加入Mg能放出H2的溶液中:Mg2+、NH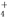 、ClO-、K+
、ClO-、K+
查看答案和解析>>
科目:高中化学 来源:2017届湖南省怀化市高三上学期期末化学试卷(解析版) 题型:选择题
用O2将HCl转化为Cl2,反应方程式为:4HCl(g)+O2(g)?2H2O(g)+2Cl2(g)△H >0 一定条件下在密闭容器中测得反应过程中n(Cl2)的实验数据如下.下列说法正确的是( )
t/min | 0 | 2 | 4 | 6 |
n(Cl2)/10﹣3 mol | 0 | 1.8 | 3.7 | 5.4 |
A.0~2 min的反应速率小于4~6 min的反应速率
B.2~6 min用Cl2表示的反应速率为0.9 mol/(L•min)
C.降低温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动。
D.平衡常数:K(200℃)<K(400℃)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com